分子構造の世界へようこそ!今日は、二酸化塩素 - clo2 ルイス 構造について掘り下げてみましょう。ClO2のルイス構造を理解することは、その結合と分子特性を理解する上で重要です。

ルイス構造とは?
Gilbert N. Lewisによって開発されたルイス構造は、分子内の原子間の結合と分子内に存在する孤立電子対を表すダイアグラムです。これらは、化合物内の電子がどのように分配されるかを視覚的に示し、分子の幾何学、混成化、極性を予測するのに役立ちます。
二酸化塩素(ClO2)とは何ですか?
二酸化塩素(ClO2)は、塩素原子1個と酸素原子2個から成る化学化合物です。室温では黄色から赤色の気体で、刺激臭があります。ClO2は、その強力な酸化特性とさまざまな微生物に対する効果的な性質から、殺菌剤、漂白剤、臭気消し剤として広く使用されています。
clo2 ルイス 構造を描く方法
clo2 ルイス 構造の描き方を探ってみましょう:
Step 1:中心原子を決定する:ClO2では、塩素(Cl)が最も電気陰性が低いため、中心原子です。
Step 2:総価電子数を計算する:塩素は7個の価電子を持ち、各酸素は6個を寄与するため、合計は7 + (2 × 6) = 19個の価電子です。
Step 3:単結合で原子を結合する:中心の塩素原子と各酸素原子の間に単結合を形成します。
Step 4:残りの電子を配置する:各酸素原子に孤立電子対を配置し、すべての価電子が使用されるまで続けます。
Step 5:オクテット則を確認する:各原子(水素以外)の周りの電子の数を数えて、外部シェルが完全であることを確認します。

clo2 ルイス 構造
二酸化塩素(ClO2)の分子幾何学
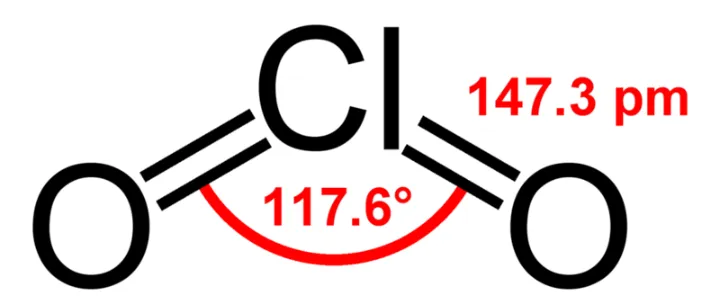
ルイス構造から、ClO2は曲がった分子幾何学を採用していることが示唆されます。中心の塩素原子の両側に酸素原子が配置され、曲がった形状が形成されます。この幾何学は、中心の塩素原子に2つの孤立電子対が存在することにより、反発が生じ、分子が曲がる結果となります。
(画像出典:ウィキペディア)
二酸化塩素(ClO2)の混成化
ClO2では、中心の塩素原子がsp3混成を受けます。塩素の1つのs軌道と3つのp軌道が混成して、四つのsp3混成軌道が形成されます。これらの軌道は、酸素原子のp軌道と重なり、二つの強力なσ結合と二つの孤立電子対が形成され、曲がった分子幾何学が生じます。
二酸化塩素(ClO2)は極性ですか、それとも非極性ですか?
二酸化塩素(ClO2)は極性分子です。個々のCl-O結合は塩素と酸素の電気陰性差により極性ですが、曲がった分子幾何学は電荷の不均等な分布をもたらし、ネットの双極子モーメントを生じます。
二酸化塩素(ClO2)のおおよその結合角と結合長は何ですか?
ClO2のおおよその結合角は約117度です。この角度は、二つの孤立電子対が存在するために生じる大きな反発により、三角平面配置の理想的な120度から逸脱します。二酸化塩素のCl-O結合の結合長は約156ピコメートル(pm)です。
注:孤立電子対の反発や結合極性などの要因により、実際の結合角や長さはわずかに異なる場合があります。
二酸化塩素のハイライト
| 二酸化塩素 Cas 10049-04-4 |
| 分子式 |
ClO2 |
| 分子形状 |
曲がった |
| 極性 |
極性 |
| 混成化 |
sp3混成化 |
| 結合角 |
117.6度 |
| 結合長 |
147.3 pm |





