-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here


Die Lewis Formel, entwickelt von Gilbert N. Lewis, stellt die Elektronenverteilung innerhalb von Molekülen visuell dar. Indem valenzelektronen als Punkte und Bindungen als Linien dargestellt werden, können diese Strukturen das Molekülabbild und dessen Eigenschaften aufgrund des Oktettregels vorhersagen, die besagt, dass Atome durch das Erreichen von acht Elektronen in ihrer äußeren Schale Stabilität suchen.
Kohlenstoffdisulfid (CS2) ist ein farbloses, brennbares Flüssigmittel, das durch seinen charakteristischen Geruch gekennzeichnet ist. Es besteht aus einem Kohlenstoffatom, das mit zwei Schwefelatomen verbunden ist, und zeigt eine lineare molekulare Struktur. Es wird hauptsächlich in der Herstellung von Farbstoffen, fotografischen Chemikalien und als Lösungsmittel verwendet.
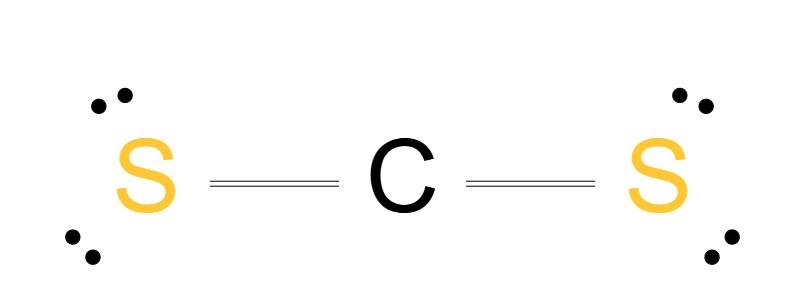
Lassen Sie uns erkunden, wie man die cs2 Lewis Formel zeichnet:
Schritt 1: Identifizieren des Zentralatoms: Kohlenstoff (C) ist das Zentralatom, da es weniger elektronegativ als Schwefel (S) ist.
Schritt 2: Zählen der Gesamtvalenzelektronen: Kohlenstoff trägt 4 Valenzelektronen bei, und jedes Schwefelatom trägt 6, was insgesamt 4 + (2 x 6) = 16 Valenzelektronen ergibt.
Schritt 3: Anordnen der Elektronen: Verbinden Sie jedes Schwefelatom mit dem zentralen Kohlenstoffatom mit einer Doppelbindung (zwei Linien) und verteilen Sie die übrigen Elektronen als Allelepaare um jedes Schwefelatom.
Schritt 4: Erfüllen des Oktettregels: Stellen Sie sicher, dass jedes Schwefelatom 8 Elektronen hat (zwei Allelepaare und eine Doppelbindung), und das Kohlenstoffatom hat 4 Elektronen (zwei Allelepaare und eine Doppelbindung).
Schritt 5: Überprüfen der Formalladungen: Formalladungen werden normalerweise nicht berücksichtigt, da der Oktettregel erfüllt ist.
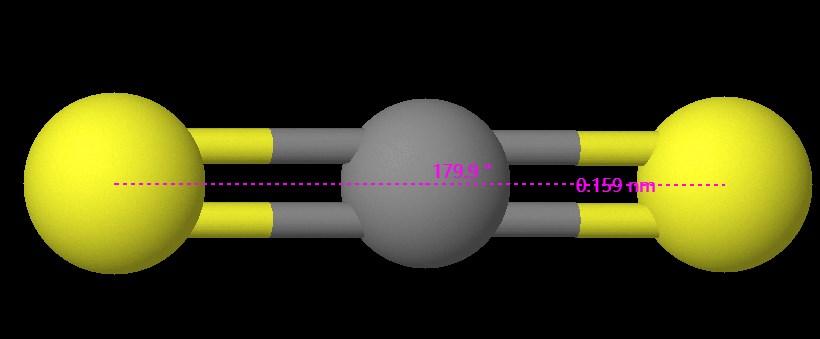
Das CS2-Molekül nimmt eine lineare Geometrie aufgrund der Anordnung der Elektronenpaare um das zentrale Kohlenstoffatom ein. Mit zwei Schwefelatomen, die an das Kohlenstoffatom gebunden sind und keine Allelepaare vorhanden sind, weist das Molekül eine lineare Form mit einem Bindungswinkel von 179,9 Grad auf.
In der molekularen Orbitaltheorie spielt die Bindung in CS2 die Überlagerung der 2s- und 2p-Orbitale der Schwefelatome mit dem 2s-Orbital des Kohlenstoffatoms eine Rolle. Dies führt zur Bildung von zwei molekularen Orbitals: dem bindenden σ2s2p und dem antibindenden π2p2s. Aufgrund des Mangels an Allelepaaren behält das Molekül eine lineare Geometrie mit einem 180-Grad-Bindungswinkel.
Die lineare Geometrie von CS2 entsteht durch die Anordnung der Elektronenpaare um das zentrale Kohlenstoffatom, wobei es einen 180-Grad-Bindungswinkel zwischen den Schwefelatomen gibt. Diese Konfiguration minimiert die Elektronenrepulsion und stabilisiert das Molekül.
In CS2 beträgt der Bindungswinkel ungefähr 179,9 Grad, was typisch für ein lineares Molekül ist. Die Bindungslänge beträgt etwa 0,159 nm und spiegelt die Stärke der C-S-Bindungen in dieser Verbindung wider.
| Kohlenstoffdisulfid (CS2) Cas 7783-06-4 | |
| Molekulare Formel | CS2 |
| Molekulare Form | Linear |
| Polarität | Unpolar |
| Hybridisierung | sp-Hybridisierung |
| Bindungswinkel | 179,9 Grad |
| Bindungslänge | 0,159 nm |
Um festzustellen, ob eine Lewis Formel polar ist, muss man die molekulare Geometrie und die Polarität der Bindungen betrachten. Bei CS2 führt die lineare Anordnung und die symmetrische Verteilung der Elektronenpaare um das zentrale Kohlenstoffatom zu einem unpolaren Molekül, da die Dipolmomente sich gegenseitig aufheben.
Um die Bindungsenergie in CS2 zu berechnen, betrachtet man die Bindungsenergie einer einzelnen C-S-Bindung, die etwa 310 kJ/mol beträgt. Da CS2 zwei C-S-Bindungen enthält, multipliziert man die Bindungsenergie mit 2, was zu einer Gesamtbindungsenergie von 620 kJ/mol für das CS2-Molekül führt.
Die Bindungsordnung in CS2 wird durch die Anzahl der chemischen Bindungen zwischen den Atomen bestimmt. Jede C-S-Bindung in der Lewis Formel stellt eine Bindungsordnung von 1 dar, was die Existenz einer einfachen Bindung zwischen Kohlenstoff und Schwefel widerspiegelt.
Bei der Bestimmung der besten Lewis Formel für CS2 ist es wichtig, sowohl die Bindungen als auch die Anordnung der Elektronen zu berücksichtigen, um die stabilste Darstellung zu gewährleisten. Die Wahl der richtigen Struktur hilft dabei, die molekularen Eigenschaften und das Verhalten zu verstehen. Wenn Sie herausfinden möchten, wie man die beste Lewis Formel für CS2 oder andere Verbindungen auswählt, bietet Guidechem Zugang zu einer breiten Palette globaler Lieferanten von Kohlenstoffdisulfid. Hier finden Sie die idealen Rohstoffe zur Unterstützung Ihrer Forschung und Anwendungen.
 |
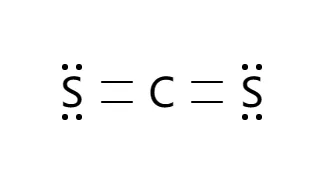 |