
분자 구조의 흥미로운 세계에 오신 것을 환영합니다! 오늘은 독특한 특성과 응용 분야를 가진 CH2Br2의 레이위스 구조를 탐구할 것입니다. 레이위스 구조를 이해함으로써 CH2Br2에서 원자가 어떻게 결합하는지 파악하고, 분자의 기하학, 하이브리드화, поля성을 이해하는 데 핵심적인 정보를 얻을 수 있습니다.
레이위스 구조는 무엇인가요?
레이위스 구조는 Gilbert N. Lewis가 제시한 시각적인 분자 전자 배치 표현입니다. вал렌스 전자를 점으로, 결합을 선으로 그려 분자의 모양과 특성을 예측합니다. 이 규칙은 원자가 외부 셀프에 8개의 전자를 가지고 있는 상태에서 안정성을 얻으려고 한다는 것을 기반으로 합니다. 레이위스 구조는 이 규칙을 준수하여 화학 결합에 대한 명확한 그림을 제공합니다.
디 브로 모 메탄은 무엇인가요?
디 브로 모 메탄 (CH2Br2)은 단일 탄소 원자와 두 개의 수소 원자, 두 개의 브롬 원자를 결합한 유기 브롬화물입니다. 무색 액체로 달콤한 향기가 있으며, 유기 합성, 용제 및 기타 화학 물질 생산 중간체로 사용됩니다.
CH2Br2 레이위스 구조 그리는 방법
CH2Br2 레이위스 구조 그리는 방법에 들어가 보겠습니다:
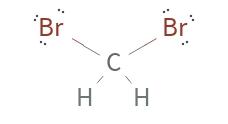
1단계: 중앙 원자를 식별하세요: 탄소(C)는 브롬보다 덜 전기음성적이며 네 개의 결합을 형성할 수 있으므로 CH2Br2의 중심 원자입니다.
2단계: 전부 전자 계산: 탄소가 4개의 전자를 공여하고, 각 수소가 1개, 각 브롬이 7개의 전자를 공여하므로 총 전자 수는 4 + (2 x 1) + (2 x 7) = 20개입니다.
3단계: 원자 주변 전자를 배치하세요: 각 수소와 브롬 원자에 단일 결합(선)으로 연결하고, 각 브롬 원자 주변에 남은 전자를 고유 전자 쌍으로 배치합니다.
4단계: 옥텟 규칙 만족: 각 브롬 원자가 8개의 전자를(3개의 고유 전자 쌍과 1개의 결합 전자 쌍) 가지도록 하며, 탄소 원자도 8개의 전자를(2개의 고유 전자 쌍과 4개의 결합 전자 쌍) 가지도록 합니다.
5단계: 공식 전위 확인: 모든 원자가 옥텟 규칙을 성취했으므로 공식 전위 검토가 필요하지 않을 수 있습니다.
디 브로 모 메탄의 분자 기하학
레이위스 구조에 따르면 CH2Br2는 사각뿔형 기하학을 갖습니다. 이 배열에서는 두 수소 원자와 두 브롬 원자가 중심 탄소 원자 주위에 대칭적으로 위치하며, 4개의 결합 쌍을 형성합니다. 이러한 기하학은 전자-전자 반발을 최소화하여 안정적인 구성을 유지합니다.

디 브로 모 메탄의 하이브리드화
CH2Br2에서 탄소 원자는 sp3 하이브리드화를 겪습니다. 하나의 s 오비탈과 세 개의 p 오비탈이 결합하여 네 개의 sp3 하이브리드 오비탈을 형성합니다. 이러한 오비탈은 수소 원자들의 s 오비탈과 브롬 원자들의 p 오비탈과 교차하여 강력한 σ 결합을 형성합니다. 이러한 하이브리드화는 CH2Br2 분자의 안정성과 대칭성을 보장합니다.
디 브로 모 메탄은极性이 있나요?
디 브로 모 메탄 (CH2Br2)은极성 분자입니다. C-H 결합은 상대적으로 무극적이지만, C-Br 결합은 탄소(2.55)와 브롬(2.96)의 전기음성성 차이로 인해 상당히极적입니다. 사각뿔형 배열로 인해 이러한极성 결합의 비대칭 분포가 발생하여 CH2Br2에 정적 전하 분산이 생깁니다.
디 브로 모 메탄의 대략적인 결합 각 및 결합 길이
CH2Br2의 결합 각은 약 109.5도입니다. 이 각은 분자의 사각뿔형 기하학에서 나오는데, 수소와 브롬 원자가 중심 탄소 원자 주위에 위치합니다. C-H의 결합 길이는 약 109pm이고, C-Br의 결합 길이는 약 189pm입니다.
참고: VSEPR 이론은 분자 기하학과 결합 각을 예측하기 위한 좋은 출발점이지만, 실제 분자는 때로는 고유 전자 쌍 반발, 결합极성, 분자의 상호 작용 등의 요인으로 인해 이상적인 각에서 벗어날 수 있습니다.
디 브로 모 메탄의 주요 특징
| 디 브로 모 메탄 Cas 74-95-3 |
| 분자 공식 |
CH2Br2 |
| 분자 모양 |
사각뿔형 |
| 극성 |
극성 |
| 하이브리드화 |
sp3 하이브리드화 |
| 결합 각 |
109.5도 |
| 결합 길이 |
C-H: 109 pm; |




