メタノールのルイス構造について深く掘り下げましょう。化学で重要なシンプルかつ重要な化合物であるメタノールを理解するためには、そのルイス構造を理解することが重要です。

ルイス構造は、ギルバート・N・ルイスによって導入されたもので、分子内の電子分布を視覚的に表現します。価電子を点と結合を線で描くことで、ルイス構造はオクテット則に基づいて分子の形状、結合、および性質についての洞察を提供します。この原則は、原子が8つの価電子を持つ安定な電子構成を得るために電子を獲得、失う、または共有すること傾向があることを示しています。
メタノール(CH3OH)は最も単純なアルコールで、炭素1つ、酸素1つ、そして水素3つを結合した構造を持っています。溶剤、冷却剤、燃料、様々な有機化合物の前駆体として広く使用されています。メタノールのルイス構造を理解することで、その化学的行動と応用を光らせることが出来ます。
ステップ5:正式な電荷の確認:オクテット則が達成されているため、全ての原子がオクテット規則を満たしている場合、正式な電荷は必要ありません。 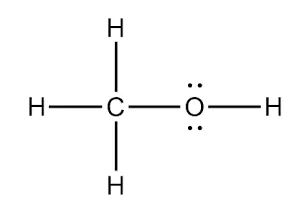
ルイス構造により、メタノールは曲線形状を取ることが示されます。酸素原子の2つの孤電子対により、直線形から逸脱し、曲線形状が生じます。この形状はその物理的と化学的性質に影響を与えます。

メタノールでは、炭素がsp3混合化を行います。一つのs軌道と三つのp軌道が組み合わさり、四つのsp3混合軌道が形成され、それらは他の原子の軌道と重なり、結合を形成します。この混合化はメタノールの安定性と構造的な強さを保証します。
メタノールは極性分子です。炭素と酸素間の電子吸収の差により、極性共鳴結合が形成されます。さらに、曲線的な分子の形状により、電荷の分配が不均衡になり、ネットドップモーメントが生じます。
注意:実際の結合角度と長さは、孤電子対の反動や結合の極性など、いくつかの要因により若干異なることがあります。
| メタノール Cas 67-56-1 | |
| 分子式 | CH4O |
| 分子形状 | - |
| 極性 | 極性 |
| ハイブリダイゼーション | sp3 ハイブリダイゼーション |
| 結合角 | 109.5 度 |
| 結合長 | 143 pm |
 |
 |