
ルイス構造は、ギルバート・N・ルイスによって考案され、分子内の電子配置を視覚的に表すものです。価電子をドットで、結合をラインで表現することで、ルイス構造は八隅則に基づいて分子の形状や特性を予測します。この規則は、原子が外殻に8つの電子を持つことで安定性を得ようとする傾向を述べています。ルイス構造はこの規則に従い、化学結合の明確な画像を提供します。
二酸化窒素(NO2)は、褐色から赤色の非常に反応性の高いガスで、窒素原子1つと酸素原子2つから成り立っています。これはさまざまな工業プロセスで一般的に使用され、硝酸の製造や光化学スモッグの形成における成分として利用されます。NO2は有毒であり、呼吸器問題を引き起こすことがあります。
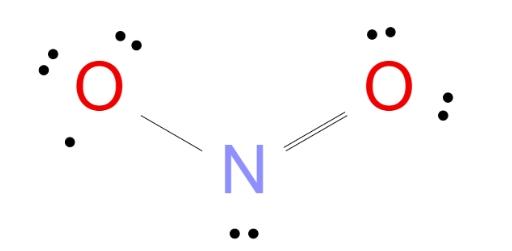
では、NO2のルイス構造を描いてみましょう:
ステップ1: 中心原子を特定する:窒素(N)は酸素よりも電気陰性度が低いため、NO2の中では中心原子となります。
ステップ2: 全ての価電子を計算する:窒素は5つの価電子を持ち、各酸素は6つずつ持つため、合計は5 + (2 x 6) = 17個の価電子になります。
ステップ3: 電子を原子周囲に配置する:各酸素原子を中心の窒素原子に単結合(線)でつなぎ、残りの電子を各酸素原子周囲の非共有電子対として配置します。
ステップ4: 八隅則を満たす:各酸素原子には8つの電子(2つの非共有電子対と1つの結合電子対)があり、窒素原子には5つの電子(1つの非共有電子対と3つの結合電子対)があります。
ステップ5: 正式電荷を確認する:形式電荷を最小限にするために構造を調整します。安定性を得るために窒素との間で1つの酸素原子が二重結合を持つべきです。
二酸化窒素の構造は、中央に窒素原子があり、それに2つの酸素原子が結合したものです。窒素原子には5つの価電子、各酸素原子には6つの価電子があり、これが曲がった分子幾何学を生じさせます。窒素原子上の非共有電子対の存在により、結合角は約120度になります。

この理論は、電子反発と化合物が安定な形態を取る必要性について説明しています。NO2においては、窒素と酸素の間には2つのシグマ結合があり、窒素上には1つの非共有電子対があります。分子軌道理論によれば、結合軌道と反結合軌道が分子全体の安定性に寄与します。
ルイス構造は、NO2が曲がった形状を取ることを示唆しています。この配列では、2つの酸素原子が中央の窒素原子の周りに位置し、約120度の結合角を持つ曲がった構造を形成します。この形状は電子-電子反発を最小限に抑え、安定な構成を実現します。
窒素と酸素分子の相互作用による混成状態を決定するために、関係する軌道と生成される結合を検討します。関係する軌道は2s、2px、2py、2pzです。基底状態にある窒素原子は、その形成過程で2s22p3の構成を持ちます。
2sおよび2px軌道内の電子対は励起状態でペアを解き、それぞれのペアの1つは空いている2pyおよび2pz軌道に昇格します。これにより、2つのsp2混成軌道と1つの未混成p軌道が生成されます。
NO2の結合角は約120度です。この角度は、分子の曲がった形状から生じ、2つの酸素原子が中央の窒素原子の周りに位置しています。NO2の結合長は約0.122 nmです。
| 二酸化窒素 ケース 10102-44-0 | |
| 分子式 | NO2 |
| 分子形状 | 曲がった形状 |
| 偏極性 | 偏極 |
| 混成状態 | sp2混成状態 |
| 結合角 | 120度 |
| 結合長 | 0.122 nm |
ルイス構造が偏極かどうかを判断するには、分子形状と結合偏極を調べます。窒素二酸化物(NO2)の場合、ルイス構造は中心に窒素が置かれ、2つの酸素原子と結合しています。NO2は曲がった形状を持ち、2つの酸素原子が窒素原子の周りに非対称に配置されています。この非対称性により、分子に純粋な偶極モーメントが生じ、NO2を偏極分子とします。
NO2の全結合エネルギーを計算するには、まず単一の窒素-酸素(N-O)結合の結合エネルギーを調べます。これは約201 kJ/molです。NO2には2つのN-O結合があるため、1つのN-O結合の結合エネルギーを結合数で掛けます。これにより、NO2の全結合エネルギーは402 kJ/molになります。この値は、1モルのNO2分子内の全てのN-O結合を破壊するのに必要なエネルギーを表します。
結合順位は、原子ペア間の化学結合の数です。NO2のルイス構造では、1つの窒素-酸素結合が単結合であり、もう1つは二重結合です。したがって、結合順位はそれぞれ1と2です。各N-O結合の平均結合順位は(1 + 2) / 2 = 1.5と計算されます。
ルイス構造における電子グループには、結合電子対(共有電子)と非結合電子対(孤電子対)が含まれます。NO2では、窒素原子の周囲には3つの電子グループがあります。これは、2つのN-O結合(2つの結合電子対と窒素上の1つの非結合電子対)に対応します。
ルイスドット構造におけるドットは、価電子を表しています。各ドットは原子の1つの価電子に対応します。NO2では、窒素は2つの結合電子対(ルイス構造では線で表される)と1つの非結合電子対(2つのドットで表される)に囲まれています。ドットは、電子がどのように共有またはペアになるかを視覚化するのに役立ちます。
 |
 |
 |