
ルイス構造は、ギルバート・N・ルイスによって考案されたもので、分子内の電子配置を視覚的に表現します。価電子をドットで示し、結合を線で示すことで、ルイス構造はオクテット則に基づいて分子の形状と性質を予測します。この則は、原子が安定性を得るためには外殻に8個の電子を持つ傾向があることを述べています。ルイス構造はこの則に従っており、化学結合の明確なイメージを提供します。
酸素(O2)は、二つの酸素原子が結合した無色、無臭、無味の二原子ガスです。それは生命にとって不可欠で、呼吸や燃焼をサポートします。酸素の分子量は32 g/molで、非常に反応性が高く、多くの化学反応に参加します。
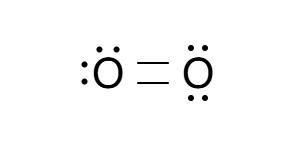
酸素(O2)のルイス構造を描く手順:
ステップ1 :中心原子の特定:両方の酸素原子は同一なので、どちらでも中心原子として選択できます。実際には両方の原子を等しく扱います。
ステップ2 :総価電子数の計算:各酸素原子は6個の価電子を持ち、合計で6 + 6 = 12個の価電子があります。
ステップ3 :原子周囲の電子の配列:二つの酸素原子を二重結合(二本の線)で結び、残りの電子を各酸素原子の周りに孤対電子として配分します。
ステップ4 :オクテット則の満足:各酸素原子が8個の電子(2個の孤対電子と2個の結合対)を持っていることを確認します。
ステップ5 :形式電荷の確認:両方の酸素原子が完全なオクテットを持っているため、形式電荷は必要ありません。

酸素の構造は、二つの酸素原子が二重結合で結ばれたものです。O2の分子幾何学は直線形であり、O-O結合の間の角度は180度です。
この理論は電子反発と化合物が安定な形態を採ることの必要性に対処します。O2では、酸素原子間には二つのπ結合と一つのσ結合が形成されます。分子軌道図では、二つの結合π軌道と二つの非結合π軌道があり、これは結合順序2に対応し、二重結合を表します。
ルイス構造によると、O2は直線形の幾何学を採用します。この配置では、二つの酸素原子が一直線上に位置し、二重結合を形成します。この幾何学は電子間の反発を最小限に抑え、安定な配置をもたらします。
参与する軌道と酸素分子間の相互作用により生成される結合を調べることで、酸素のハイブリダイゼーションを決定します。2sと2p軌道が関与します。酸素原子は基底状態で、その形成時には2s22p4の構成を持ちます。
基底状態から励起状態になると、2sと2p軌道の電子ペアがアンパアレントになり、それぞれのペアの一つが空いている2p軌道に促進されます。現在では、一つの2sと二つの2pの半分の軌道がハイブリダイズし、二つのsp2ハイブリッド軌道が生成されます。
O2の結合角は約180度です。これは、分子が直線形であるためで、二つの酸素原子が一直線上に位置することで180度の結合角が生じます。O2の結合長は約120.7 pmです。
| 酸素 CAS 7782-44-7 | |
| 分子式 | O2 |
| 分子形状 | 直線形 |
| 極性 | 非極性 |
| ハイブリダイゼーション | sp2ハイブリダイゼーション |
| 結合角 | 180度 |
| 結合長 | 120.7 pm |
ルイス構造が極性かどうかを判断するには、分子の幾何学と結合の極性を検討します。酸素(O2)の場合、ルイス構造は二つの酸素原子が二重結合で結ばれています。O2は直線形の幾何学を持ち、二つの酸素原子が対称的に配置されています。O-O結合は極性ですが、分子の対称性により双極モーメントが打ち消され、O2は非極性分子となります。
O2の結合エネルギーを計算するには、単一の酸素-酸素(O-O)結合の結合エネルギーを調べます。これは約498 kJ/molです。O2は一つのO=O二重結合を持っていますので、O=O結合のエネルギーを二重結合の数で掛けます。これにより、O2の結合エネルギーは498 kJ/molとなります。これは1モルのO2分子のO=O結合を切断するのに必要なエネルギーを表します。
結合順序は、原子ペア間の化学結合の数を表します。O2のルイス構造では、二つの酸素原子が二重結合で結ばれています。したがって、O-O結合の結合順序は2です。レゾナンストラクチャーがある場合は、結合順序は異なる構造の平均値になりますが、O2にはレゾナンストラクチャーがないため、結合順序は2のままです。
ルイス構造における電子グループは、原子周囲の共有電子対(結合対)と非共有電子対(孤対)を含みます。O2では、各酸素原子には二つの電子グループがあります。これは二つのO-O結合(二つの結合対と酸素上には孤対が存在しない)に対応しています。
ルイス点構造において、点は価電子を表します。各点は原子の一つの価電子に対応します。O2では、各酸素原子は三組の点(孤対)と他の酸素原子との一つの結合対を表します。点は原子間での電子の共有やペアリングを視覚化するために使用されます。
 |
 |
 |