-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here

환영합니다! 매력적인 분자 구조의 세계에 오신 것을 환영합니다! 오늘은 화학에서 흥미로운 특성과 의미를 지닌 분자 구조의 매혹적인 세계에 오신 것을 환영합니다! 오늘은 화학에서 흥미로운 특성과 의미를 지닌 산화물 삼산화물(SeO3)의 루이스 구조를 살펴보겠습니다. SeO3의 루이스 구조는 결합, 구조 및 기타 중요한 특성을 이해하는 데 도움이 됩니다.

루이스 구조는 가일버트 N. 루이스가 개발한 분자의 결합을 시각화하는 그림입니다. 이 그림은 원자를 구성하는 valence 전자들의 배열과 분자의 모양, 성질을 예측하는데 도움이 됩니다. 오케타르 규칙에 따라 원자가 외부 원자 셀리스에 8개의 전자를 얻거나 잃거나 나누어 안정한 전자 구조를 이루려는 경향을 보여줍니다.
산화 삼산화(SeO3)는 한 개의 세일렌 원자와 세 개의 산소 원자로 구성된 화학물질입니다. 실내 온도에서는 무색 고체이며, 유기 합성에 중요한 재агент으로 사용됩니다, 특히 유기 화합물의 산화에.
이제 SeO3의 루이스 구조를 그리는 방법을 살펴보겠습니다:
1단계: 중앙 원자 결정: Se(세일렌)이 SeO3의 중앙 원자입니다. Se는 산소보다 더 많은 결합을 형성할 수 있기 때문입니다.
2단계: 총 valence 전자 계산: Se는 6개의 valence 전자를 제공하고, 각 산소는 6개, 총 6 + (3 x 6) = 24개의 valence 전자를 갖습니다.
3단계: 원자 주변에 전자를 배치: 각 산소 원자와 중앙 세일렌 원자 사이에 단일 결합선(선)을 두고, 모든 산소 원자 주변에 남은 전자를 빈자리로 배치합니다.
4단계: 오케타르 규칙 준수: 각 산소 원자가 8개의 전자(2개의 빈자리와 2개의 결합자리)를 가지고, 세일렌 원자가 12개의 전자(6개의 결합자리)를 얻도록 합니다.
5단계: 공식전하 확인: 공식전하가 필요하지 않을 수도 있습니다. 모든 원자가 오케타르 규칙을 준수하고 있기 때문입니다.
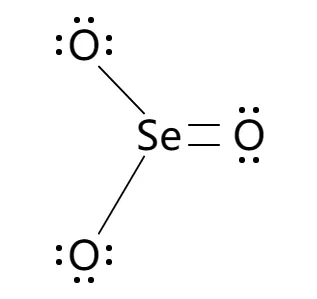
루이스 구조는 SeO3가 삼각 피라미드형 구조를 따릅니다. 여기서 산소 원자들은 중앙 세일렌 원자 주변에 불균형하게 배치되어 있으며, 한 개의 빈자리와 두 개의 결합자리가 있습니다. 이러한 구조는 전자-전자 상호 작용 최소화로 안정성을 유지합니다.

SeO3에서 세일렌 원자는 sp3 하이브리지레이션을 거칩니다. 한 개의 s-orBITAL과 세 개의 p-orBITAL이 네 개의 sp3 하이브리지 오비탈을 형성합니다. 이 오비탈들은 산소 원자의 p 오비탈과 겹쳐서 강한 σ 결합을 형성합니다. 이 하이브리지레이션은 SeO3 분자의 안정성과 정규성을 보장합니다.
산화 삼산화(SeO3)는 극성 분자입니다. 세일렌과 산소 원자 간의 전자 차이로 인해 전기적 극성이 있지만, 중앙 세일렌 원자 주변에 산소 원자들의 비대칭 배치로는 전자 분포의 균형을 깨지며 극성 분자로 나타납니다.
SeO3의 각도는 대략 107도입니다. 이 각도는 분자의 삼각 피라미드 구조에서 빈자리의 반발력으로 약간 감소하여 정상적인 109.5도보다 작게 됩니다. 세일렌과 산소 원자 사이의 결합거리는 대략 160 페인미터입니다.
참고: 진정한 각도와 길이는 빈자리 반발력 및 분자 상호작용 등의 요인에 따라 약간 변동할 수 있습니다.
| 산화 삼산화(Cas 13768-86-0) | |
| 분자 식 | SeO3 |
| 분자 모양 | 삼각 피라미드형 |
| 극성/비극성 | 극성 |
| 하이브리지레이션 | sp3 하이브리지레이션 |
| 각도 | 107° |
| 결합거리 | 160 pm |
 |