
분자 구조의 흥미로운 세계에 오신 것을 환영합니다! 오늘은 독특한 특성과 응용 분야를 가진 ClO3 레위스 구조 분자 기하학을 탐구할 것입니다. 레위스 구조를 이해하면 ClO3에서 원자가 어떻게 결합하는지 설명하고 분자 기하, 하이브리드화, поля성을 파악하는 데 도움이 됩니다.
레위스 구조는 무엇인가요?
Gilbert N. Lewis가 제안한 레위스 구조는 분자의 전자 배치를 시각적으로 나타내는 방법입니다. 와전자를 점으로, 화학결합을 선으로 표시하여 이동 규칙을 기반으로 분자의 모양과 특성을 예측합니다. 이 규칙은 원자가 외부 셀에 8개의 전자를 가지고 있으면 안정성이 가장 높다는 것을 말합니다. 레위스 구조는 이 규칙을 준수하며 화학결합에 대한 명확한 그림을 제공합니다.
클로르인 삼산화물은 무엇인가요?
클로르인 삼산화물(ClO3)은 하나의 클로린 원자와 세 개의 산소 원자를 결합한 화합물입니다. 그 특이한 반응성으로 유명하며 다양한 화학 반응과 산업 프로세스에 사용됩니다. 클로르인 삼산화물은 산화 특성으로 인해 화학 분야에서 중요한 역할을 합니다.
ClO3 레위스 구조 분자 기하학 그리기
이동 규칙을 준수하는 ClO3 레위스 구조 그리기에 뛰어들어봅시다:
1. 중앙 원자 식별: 클로린(Cl)이 산소보다 덜 전기 음성적이므로 Cl이 중앙 원자입니다.
2. 전자 수 계산: 클로린이 7개의 와전자를, 각 산소가 6개의 와전자를 공헌하므로 총 전자 수는 7 + (3 x 6) = 25개입니다.
3. 원자 주위에 전자를 배치: 각 산소 원자와 중앙 클로린 원자 사이에 단일 결합(선)으로 연결하고, 각 산소 원자 주위에 남은 전자를 고유의 쌍으로 배치합니다.
4. 이동 규칙 충족: 각 산소 원자가 8개의 전자를(2개의 고유 쌍과 1개의 결합 쌍) 가지고 있고, 클로린 원자도 8개 이상의 전자를 가질 수 있도록(확장된 이동 규칙) 25개의 와전자를 수용합니다.
5. 형식적 전荷 확인: 형식적 전荷을 최소화하기 위해 필요할 수 있으며, 일반적으로 더 정확한 분자의 표현을 제공합니다.
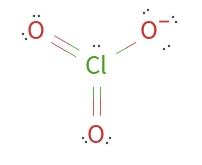
ClO3 레위스 구조 분자 기하학
클로르인 삼산화물의 분자 기하학
레위스 구조에 따르면, ClO3는 삼각뿔형 기하를 가지게 됩니다. 이 배열에서는 세 개의 산소 원자가 중앙 클로린 원자 주위에 대칭적으로 위치하며, 클로린 원자에는 한 쌍의 고유 쌍이 있습니다. 이러한 기하학은 전자-전자 반발을 최소화하여 안정적인 구성을 유지합니다.

클로르인 삼산화물의 하이브리드화
ClO3에서 클로린 원자는 sp3 하이브리드화를 거칩니다. 하나의 s 오비탈과 세 개의 p 오비탈이 결합하여 네 개의 sp3 하이브리드 오비탈을 형성합니다. 이 중 세 개의 하이브리드 오비탈이 산소 원자의 p 오비탈과 겹쳐 세 개의 강한 σ 결합을 형성합니다. 나머지 하이브리드 오비탈에는 클로린 원자에 있는 고유 쌍의 전자가 포함되어 있습니다.
클로르인 삼산화물은极性인가요? 불극성인가요?
클로르인 삼산화물(ClO3)은 평행인 분자입니다. 클로린(3.16)과 산소(3.44) 사이의 상당한 전기 음성성 차이로 인해 클로린과 산소 원자 사이에 평행인 공유결합이 있습니다. 또한 분자의 비대칭 형태로 인해 전체 분극矩이 발생하여 ClO3가 평행인 분자임을 나타냅니다.
클로르인 삼산화물의 약간의 결합 각도와 결합 길이
ClO3의 결합 각도는 약 107도입니다. 이 각도는 분자의 삼각뿔형 기하학에서 발생하는데, 세 개의 산소 원자가 중앙 클로린 원자 주위에 위치하며, 고유 쌍의 전자가 결합 각도에 영향을 미칩니다. ClO3의 결합 길이는 일반적으로 170pm 정도로 다양하지만 변동할 수 있습니다.
참고: VSEPR 이론은 분자 기하학과 결합 각도를 예측하는 좋은 시작점이지만, 실제 분자는 때로는 이deal 각도에서 벗어날 수 있습니다. 고유 쌍의 반발, 결합极성, 분자의 상호작용 등의 요인으로 인해 발생합니다.




