ペンタフルオロピリジン、別名パーフルオロピリジンは、化学式C5F5Nで表される化合物であり、CAS番号:700-16-3です。この化合物は、六員環の芳香族環を特徴とし、炭素原子上のすべての水素原子がフッ素原子によって置換されています。フッ素原子や異種元素の導入により、その分子構造と電子分布が大きく変化します。この変化により、ペンタフルオロピリジンには独自の物理化学的性質がもたらされ、励起メカニズムと緩和プロセスに影響を与えます。フッ素原子やラジカルの導入は原子核の質量を増加させ、これにより励起エネルギーが低下し、ベンゼンと比較して吸収スペクトルでは赤色シフトが生じます。さらに、フッ素原子は芳香族環またはヘテロ環におけるπ結合と反π結合の特性を強化します。フッ素原子の数が増えるにつれて、C—F結合の長さは徐々に短くなり、フッ素化芳香族化合物の分子構造はより安定し、芳香性が高まります。
ペンタフルオロピリジンの合成は、1960年代初頭に初めて報告されました。この過程では、パーフルオロピペリジンの脱フッ素化が行われました。この過程では、電気化学合成により鉄やニッケルなどの金属を用いて高温度下でピリジンと無水フッ化水素を反応させてパーフルオロピペリジンを作製しました。その後、クロマトグラフィーによる分離によりペンタフルオロピリジンを得ました。鉄を還元剤として使用した場合、ペンタフルオロピリジンの収率は26%でした。一方、ニッケルを使用した場合は収率が若干低く、12%でした。
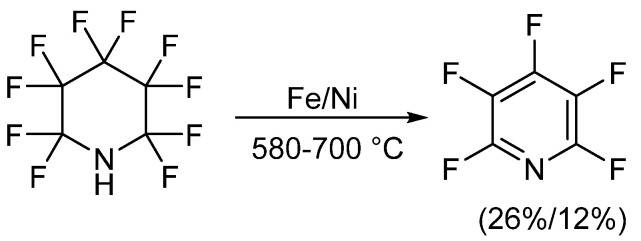
1964年と1965年に、ChambersらとBanksらはそれぞれペンタフルオロピリジンの類似の合成法を発表しました。著者たちは、高圧容器内で五塩化ピリジンと無水カリウムフッ化物を加熱してペンタフルオロピリジンを生成しました。五塩化ピリジンはピリジンと五塩化リンとの反応により作製されます。この方法では混合物が生成されますが、蒸留により分離することができます。
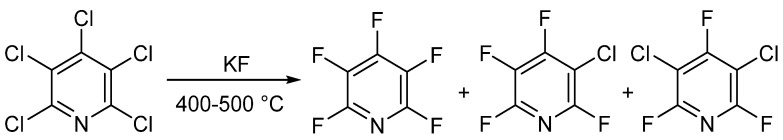
ハロゲン化物の総収量は約90%で、温度と反応時間の変更により生成物比を調整できます。最適な条件下では、ペンタフルオロピリジンの収率は83%でした。この方法は、現在でもペンタフルオロピリジンの商業合成の基準となっています。
1960年代半ば以降、ペンタフルオロピリジンの合成法に関してほとんど進展はありませんでした。約20年後、Banksらは窒素保護下で五フッ素(三塩化メチル)ベンゼンと4-ジクロロアミノテトラフッソピリジンを熱分解して微量のペンタフルオロピリジンを得ました。同じ年、CoeとSleighは鉄存在下で様々なピロリジンを熱分解しました。この反応はBanksの報告と同様に、ペンタフルオロピリジンの収率は非常に低いものでした。
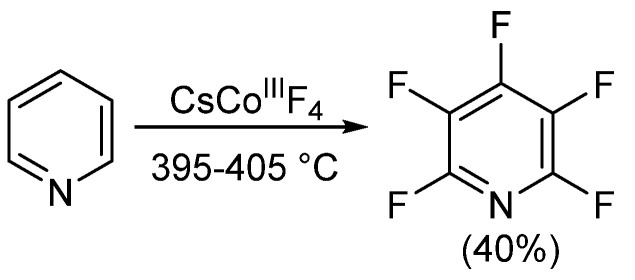
2004年、Bardinらは、鉄または亜鉛の存在下でC5Cl4F5Nの脱ハロゲン化によりペンタフルオロピリジンを得る最終例を発表しました。すべてのケースで、生成物の混合物が得られ、分離されていない収率は以下の表に示すようにGLC分析で決定されました。
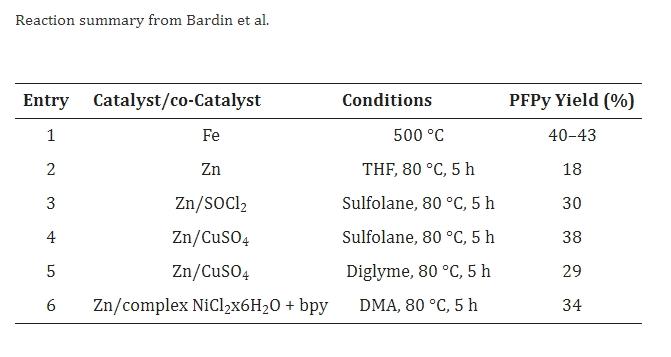
2,4,6-トリフルオロ-3,5-ジクロロピリジンを原料として、KFをフルオリン化剤として使用したZhong Xuhuiらは、ペンタフルオロピリジンの合成に注力しました。フルオリン化反応触媒に関する研究を通じて、反応温度を低減する新しい触媒を選別し、難しいフルオリン化反応の工業化への基盤を築きました。実験メカニズムを探ることで、3:1の質量比で四フェニルホスホニウムブロミドと無水AlCl3の新しい複合触媒が発見され、2,4,6-トリフルオロ-3,5-ジクロロピリジンとKFをフルオリン化剤として使用した反応で有利な実験結果が得られました。実験パラメータの最適化により、KF: トリフルオロジクロロピリジン: 四フェニルホスホニウムブロミド: AlCl3 = 30g: 150g: 3g: 1g、反応温度240°C、反応時間20時間で、3-クロロテトラフルオロピリジンが15%、ペンタフルオロピリジンが10%、触媒選択性が50%でした。
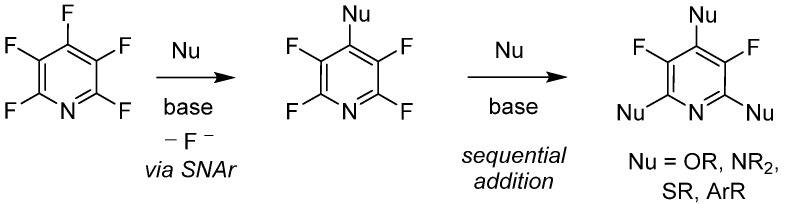
ペンタフルオロピリジンの化学的変換はよく記録されており、CF結合の活性化、光酸化還元反応、脱フルオロ化、求核的付加などの注目すべき方法が含まれています。求核試薬の種類が豊富で、既知の化学的変換は非常に柔軟です。さらに、ペンタフルオロピリジンは独特の位置選択性を示し、4位での交換的付加が穏やかな塩基条件下で顕著であり、O-、N-、S-、C-型の求核試薬が使われます。2,6-順序付加も達成可能で、3,5-二置換は個別に起こります。
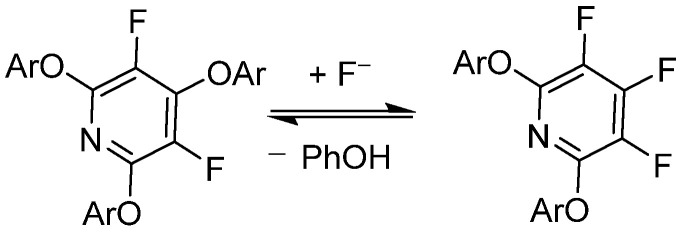
Vlasovらの研究によると、ペンタフルオロピリジンは、塩基条件下でフルオリウム(F?)と可逆的な置換反応を起こすことが示されています。フェノールなどの良好な求核試薬によって促進されます。さらに、DFTモデリングを使用した研究では、ペンタフルオロピリジンの2,6位での電子豊富および電子貧弱な芳香族エーテルの可逆的置換効果が調査されました。Brittainらはこれらの結果を利用し、ペンタフルオロピリジンをさまざまなフェノール化合物の効果的な保護基として使用し、穏やかな条件下で切断または脱保護反応を行いました。
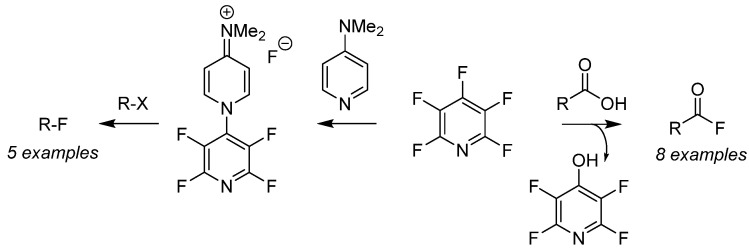
ペンタフルオロピリジンは、アルキルハライド(図の右から左)やカルボン酸の脱酸素(図の左から右)に対する求核的フルオリン化試薬として使用され、機能的基質群の準備に使用されます。ペンタフルオロピリジンとN,N-ジメチルアミノピリジンの添加により、空気安定なフルオリン化塩が生成され、有機ハライド(R-X)のフルオリン化が可能になります。さらに、ペンタフルオロピリジンとカルボン酸との求核的付加により、アシルフルオリウムが現場で生成されます。その後、エステル中間体は非キレートフルオリウムから切断され、フェノールが副生成物として得られ、目的のアシルフルオリウムが得られます。この戦略は、ペンタフルオロピリジンをカップリング剤として使用し、アミドやエステルのワンポット合成にも応用されます。
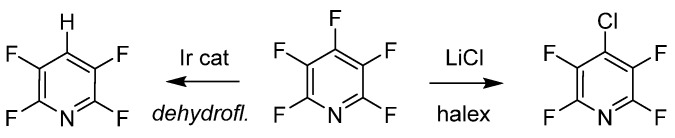
ペンタフルオロピリジンの目的に応じた操作には、位置選択的脱ハロゲン化およびハロゲン交換(Halex)が含まれます。これらのプロセスは反応条件によって位置選択的な置換を生成します。Senaweeraらはフローリアクター設計を使用して、低いIr複合体負荷で光触媒的なターンオーバーを達成し、有用な中間体のスケールアップ可能性を示しました。Halex反転置換は、ペンタフルオロピリジンの4位でLiClを用いて達成され、さらに塩素との交換は、動力学および熱力学によって制御されました。
 |