フェナジン誘導体は、その広範な生物学的活性により薬理学的に重要な位置を占めています。天然のフェナジンの顕著な薬理学的性質は、類似またはさらには改良された性質を持つ合成類縁体の設計と開発を推進しました。様々な合成フェナジン類縁体は、マラリヤ、トリパノソーマ症、肝炎Cウイルス複製抑制、がん、真菌症、レーシマンイア症、および昆虫に対する活性を有しています。また、フェナジンは有機フィールド効果トランジスタ(OFET)、有機発光ダイオード(OLED)、染料感受型太陽電池、フォトカタリストによるフォトアクティブ材料、そしてサブセルラー構造や生物学的イベントの蛍光トレーサーおよび染料としても使用されています。さらに、蛍光フェナジンは光動力療法(PDT)で感光剤として使用され、光と感光剤の組み合わせは腫瘍近くで高反応性酸素またはヒドロキシルラジカルを生成し、標的組織を選択的に破壊します。
フェナジン骨格は医療や産業における広範な応用から魅力的な合成目標となっています。フェナジンの合成方法には、Wohl-Aue法、Beirut法、1,2-ジアミノベンゼンと2Cユニットの縮合、ジフェニルアミンの還元環化、1,2-ジアミノベンゼン/ジフェニルアミンの酸化環化、Pd触媒によるN-アルキル化、および多成分反応などがあります。
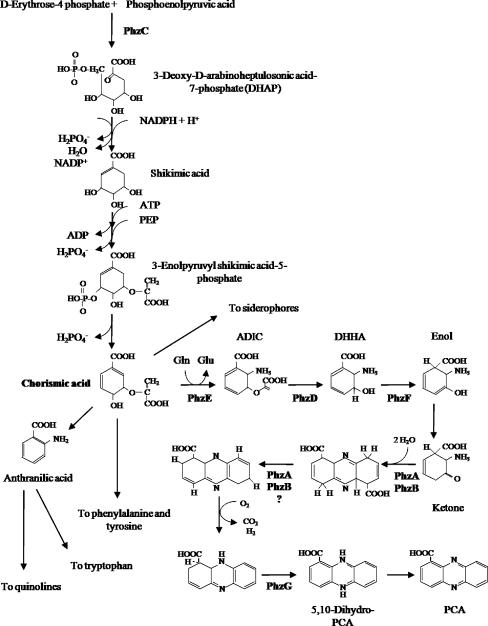
フェナジンの生合成について簡単に述べます。フェナジンはシュキミック酸経路から始まり、中間体の分岐酸を基にフェナジン芳香族構造の基本的な生合成分岐点となります。シュキミック酸生合成経路は非常に保存されており、主要な成長に必要な多くの代謝物、すなわち三つの芳香族アミノ酸とp-アミノ安息香酸の生産に関与しています。細菌ではこの経路は厳密に調節されており、最初のステップで3-デオキシ-D-アラビノヘプトローザン-7-リン酸(DAHP)合成酵素がエリスロース-4-リン酸とホスホエンオルトピルピル酸とのコンドensationを触媒します。多くの細菌は型I DAHP合成酵素同工型を持っていますが、これらは各々の最終生成物によるフィードバック阻害を受けます。興味深いことに、様々なフェナジン産生微生物では、phzC生合成オペロンによってコードされる型II-3-DAHP合成酵素は、Solanaceae植物のDAHP合成酵素に近い酵素特性を持ち、プロカルリックDAHP合成酵素とは異なります。植物では、型II-3-DAHP合成酵素は制御可能な循環構造を持たず、三つの芳香族アミノ酸生成物による調節を受けません。しかし、種子発芽、枝条の伸長、グリホサート暴露などの特定の植物成長段階において、その活性は増加します。phzCの発現は、フェナジン合成に必要な基質の十分な供給を確保するのに役立つ可能性があります。ただし、phzCの非制御発現は、主要な成長に必要な必須代謝物を枯渇させ、根域全体の適応力を低下させる可能性があります。これは、フェナジン生産の複雑な調節の一部を説明しています。

伝統的には、フェナジンとその誘導体の合成には有毒な有機溶媒、危険な試薬、そして最終製品中の有害金属汚染のリスクを伴う化学的方法が用いられてきました。これらの欠点は、フェナジン誘導体の治療および製薬産業における幅広い適用を大幅に制限してきました。そのため、環境に優しい方法の必要性が高まっています。これらはこれらの課題に対処し、環境への損傷を減らすために使用できます。現在では、機械合成、溶剤なし・触媒なし合成、グリーン溶剤合成、超音波アシスト合成、マイクロ波アシスト合成などの環境に優しい方法がフェナジンとその誘導体の合成に利用されています。これらの方法は、フェナジン骨格が生物活性成分として広く存在し、危険な溶剤、触媒、エネルギー使用量を減らす必要性が高まっているためです。
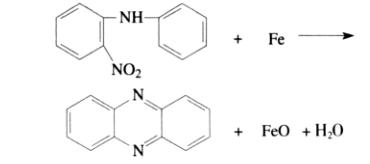
Henryは、鉄粉存在下でN-フェニル-2-ニトロアニリンを反応させ、フェナジンを得ました。収率は46%でした。ニトロ基はまずアミノ基に還元され、その後酸化環化反応によりフェナジンが生成されました。
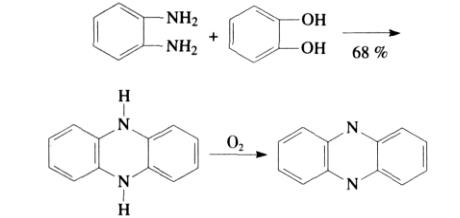
Morleyらは、以前の研究方法に基づき、カテコールとオルト-ジアミノベンゼンを反応させ、フェナジンおよびその誘導体である5,10-ジヒドロフェナジンを得ました。この過程は、200~210℃で35~40時間の圧力条件下で密閉容器内で行われました。中間生成物は5,10-ジヒドロフェナジンで、精製後粗収率は約60%でした。その後、酸素を通すことで5,10-ジヒドロフェナジンはフェナジンに変換されました。この方法の主な欠点は、大規模な生産が困難であり、多くの未検出の副生成物が生成されることです。
Watayaは、2-ニトロアニリンまたはその置換化合物を強アルカリ性金属アルコキサイドとジメチルスルホキサイド中で環化させることでフェナジンを得ました。ジメチルスルホキサイドは比較的高価な溶媒ですが、ベンゼン、トルエン、エーテル、脂肪族アルコールなどの他の溶媒は、反応が遅い、または低い収率しか得られないか、あるいは純化が困難でカラムクロマトグラフィーが必要となり、化学合成の生産コストが上昇します。
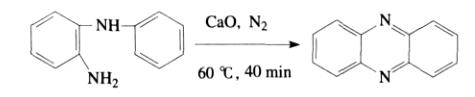
Horaguchiらは、窒素ガス保護下でカルシウム酸化物を触媒として600℃で40分間2-アミノジフェニルアミンを反応させることで、70%の収率でフェナジンを得ました。