ビンドリンの合成は、化学研究の中で挑戦的かつ重要な分野であり、その手法と技術は絶え間ない注目を集めています。継続的な実験と探求を通じて、科学者たちはビンドリンの合成経路を徐々に明らかにし、その工業生産や薬物開発における重要な参考資料と指針を提供しています。
ビンカミンおよびビンクリスチンは、インドールアルカロイドファミリーの広く認識されたメンバーで、主に抗がん剤として使用されています。これらは現在、カタランタス・ローゼウスから抽出されており、この植物が唯一の自然源となっています。しかし、この植物における含有量が低いため(数十万分の一から百万分の一の範囲)、化学的合成は経済的に不可能であり、市場価格が高騰しています。これらの薬剤は、投与量に依存する神経毒性の副作用があるため、適用範囲は限られていますが、医薬化学者たちは化学的合成や構造の改良による効率的で毒性の少ない類似物の開発を続けています。また、生物学者たちは、これらの薬剤を生産するための植物組織培養方法も探求しています。
1960年代から、カタランタス・ローゼウスの組織培養を用いたインドールアルカロイドの生産に関する研究が続けられてきました。1970年代後半の研究では、この方法を使用してこれらのアルカロイドを生産しようとしましたが、現在のところ、アジマリシン、サーペンチン、カタランチンのみが生産可能であり、産業規模での生産は実現していません。ビンドリンは、ビンカミンまたはビンクリスチンの半合成において重要な前駆体であり、植物細胞培養による大規模生産が半合成を可能にします。したがって、カタランチンとビンドリンという2つの原材料が植物細胞培養によって大量に生産されれば、ビンカミンの半合成が可能になります。ビンドリンの構造は以下の図に示されています。
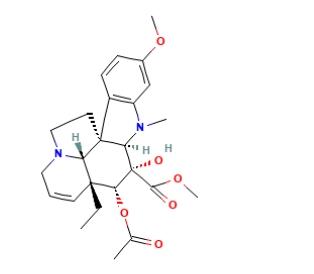
ビンドリンは、主に2つの方法で合成できます:
(1) 環化反応:これらの反応は、2つの分子を接続して新しい環を形成します。ボガー合成は、ビンドリンのコア構造に3つの環を同時に生成するタンデム[4+2]/[3+2]環化カスケードを用いた注目すべき例です。
(2) 立体選択的反応:ビンドリンには複数の立体中心(特定の空間配置を持つ原子)があり、化学者は合成中にこれらの中心の正しい三次元配置を確保するためにさまざまな技術を使用します。エナンチオ選択的触媒反応やキラル出発物質を利用する戦略が用いられます。
(3) 官能基操作:合成過程で、化学者はさまざまな官能基(例えばカルボニル基、エーテル基)を導入し、還元、脱水、保護/脱保護反応を通じてそれらを戦略的に操作して、最終的なビンドリンの構造を得ます。
(1) 代謝工学:科学者たちは、カタランタス・ローゼウス(マダガスカル・ピンクフラワー)のビンドリン生合成経路の遺伝子を酵母に導入し、これにより酵母はタベルソニンのような単純な前駆体をビンドリンに変換する酵素的能力を持ちます。
化学合成に比べて、生物合成はビンドリンの生産においてより持続可能でスケーラブルな方法を提供する可能性があります。
ビンドリンの生合成は、カタランタス・ローゼウスにおいて発見された複雑な自然の過程です。この過程には、テルペノイド中間体であるストリクトシジンから始まるいくつかの酵素触媒反応が関与しています。主な酵素は以下の通りです:
- ゲラニオール合成酵素(GES)
- ゲラニオール8-ヒドロキシラーゼ
- 8-ヒドロキシゲラニオール酸化還元酵素(GOR)
- セコロガニン合成酵素
- タベルソニン3-ヒドロキシラーゼ
- タベルソニン3-還元酵素
- 3-ヒドロキシ-16-メトキシ-2,3-ジヒドロタベルソニン-N-メチルトランスフェラーゼ(NMT)
- デサセトキシビンドリン-4-ヒドロキシラーゼ(D4H)
- デアセチルビンドリン-4-O-アセチルトランスフェラーゼ(DAT)
これらの酵素は、セコロガニンからビンドリンへと変換する過程で、ヒドロキシル化、酸化、環化、メチル化、アセチル化反応を順に進行させます。
この文脈におけるバイオ触媒とは、上記の酵素を指します。各酵素は触媒として働く特定のタンパク質であり、特定の化学反応を加速させ、消費されることはありません。これらはビンドリン合成において重要な役割を果たします:
(1) 選択性:酵素は非常に選択的であり、特定の基質にのみ作用し、望ましい反応を促進します。これにより、不必要な副反応を最小限に抑え、効率的なビンドリン形成を可能にします。従来の化学合成と比較して、酵素は穏やかな条件(温度、圧力、pH)で働き、エネルギー消費を削減し、プロセスをより環境に優しくします。
(2) ステレオ制御:多くの酵素は生成物分子の立体化学を制御することができます。ビンドリンは複数のキラル中心を持つ特定の3D構造を有します。酵素はこれらの中心の正しい配置を確保し、最終的な製品の生物学的活性にとって重要です。
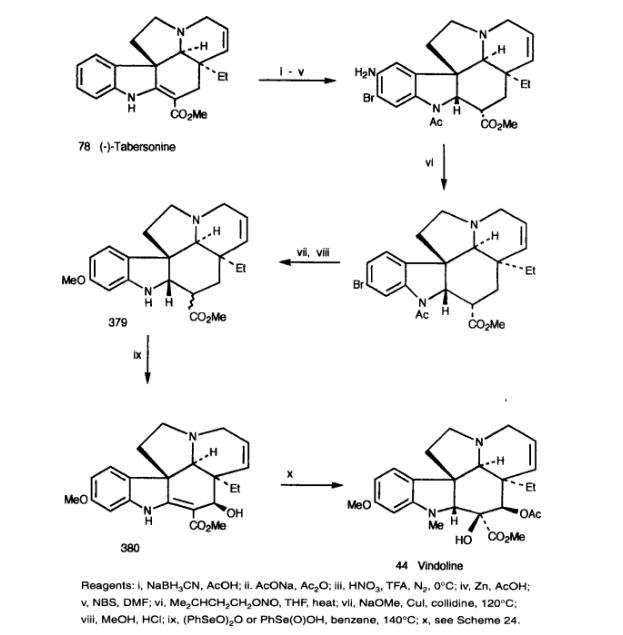
Danieliらは、豊富に存在するタベルソニンを11-メトキシタベルソニンに変換し、さらにビンドリンに変換する方法を開発しました。タベルソニンおよび2,16-ジヒドロキシタベルソニンの求電子的置換が効果的でないため、N-アセチル-2,16-ジヒドロキシタベルソニンが基質として選ばれました。ニトロ化反応により高収率で10-ニトロ誘導体が得られ、次に標準的な方法で11-メトキシ-2,16-ジヒドロキシタベルソニン(379)が得られました。生成物380をベンジルセレニウムで脱水素化しようとしたところ、期待通りC-17 β-ヒドロキシ基が導入されました。最終的に生成物380は、前述のカタランチン合成法を用いてビンドリンに変換されました。
(1) カタランタス・ローゼウスカルスの取得
カタランタス・ローゼウスの若い茎をエクスプラントとして使用し、70%エタノールで30〜50秒間表面消毒した後、5〜15%の次亜塩素酸ナトリウム溶液で10〜20分間二次消毒を行いました。その後、滅菌水で3回洗浄し、ラミナーフローキャビネットで茎を2mmのセグメントに切断しました。これらのセグメントを分化抑制培養基に接種し、25°Cで1日12〜16時間、2000 lxの光強度で3〜4週間培養して、白色カルス組織を得ました。カルス組織はさらにこの培養基で3回以上サブカルチャーし、速く成長し、柔らかい組織で安定した細胞系を選択しました。
(2) 分化抑制培養基の準備
インドール-3-酢酸(IAA)1.0 mg/Lとサイトキニン6-ベンジルアミノプリン(6-BA)1.0 mg/Lをムラシゲ・スコーグ(MS)培養基に加え、20 g/Lのスクロースを補充しました。pHは酸またはアルカリで5.8に調整し、次に6.5 g/Lの寒天を加えました。この培養基は115°C、0.1 MPaで15分間オートクレーブ処理し、冷却後にスラント状の分化抑制培養基を準備しました。
(3) カタランタス・ローゼウスカルスのサブカルチャー
誘導されたカルス細胞系は、3回以上、前述のサブカルチャー培養基でサブカルチャーされました。サブカルチャー条件は、20°C、光を避け、サブカルチャー期間は3週間です。サブカルチャー中に、構造が緩い、速く成長するカルス組織を選択して、さらにサブカルチャーしました。
(4) カタランタス・ローゼウス多倍体細胞の誘導
前述の手順で得られたカタランタス・ローゼウスカルス組織は、10 mg/Lコルヒチンを含む誘導培養基に接種しました。誘導培養は100 rpmで20°C、暗所で7日間シェイクしました。その後、細胞を収穫し、コルヒチンを含まないサブカルチャー培養基で少なくとも3回サブカルチャーしました。得られた速く成長する細胞系(培養期間中に初期接種量の5倍以上の成長率を示す)は、アセトオルセイン染色または銀染色後、顕微鏡検査で混合多倍体細胞系として確認されました。
(5) カタランタス・ローゼウス多倍体細胞の増殖培養
前述のステップで得られた活発に成長する多倍体細胞系は、増殖培養基に接種されました。25°C、暗所で3週間培養した後、初期接種量の10倍以上の細胞培養が得られました。
活発に成長する多倍体カタランタス・ローゼウス細胞系は、200 g/Lの濃度で合成培養基に接種されました。懸濁培養は25°Cで90 rpm、暗所で7日間シェイクし、ビンドリンに富む細胞を得ました。細胞を収穫した後、培養基は調整してバイオリアクターで再利用可能です。
合成培養基の準備:30 g/Lのスクロース、1 mg/Lのインドール-3-酢酸(IAA)、1 mg/Lのキネチン(KT)を改良MS培養基に加えました。pHは酸またはアルカリで5.8に調整し、次に4.5 g/Lの寒天を加えました。培養基は115°C、0.1 MPaで15分間オートクレーブ処理し、冷却しました。冷却後、フィルタリングして滅菌した前駆体化合物(アセチルコエンザイムA 10 μg/L、フェニルアラニン0.5 μmol/L、トリプタミン5 μmol/L、酢酸無水物10 μl/L、ジチオスレイトール10 mg/L)を加え、pHを5.8に調整して合成培養基を準備しました。
培養中に合成されたビンドリンに富む細胞は、抽出タンクに入れて、300 rpmで高速度で攪拌し、細胞を破壊しました。95%エタノール溶液(新鮮細胞重1gあたり1 ml)を加え、室温で抽出します。粗抽出物は真空濃縮(0.01 MPa)で得た後、2倍量のエチルアセテートを加え、pHを硫酸で8.0に調整し、急速に振とうしてアルカロイドを3回抽出しました。ビンドリンを含む混合物は真空乾燥で得られます。高性能液体クロマトグラフィー(HPLC)を用いてこの混合物中のビンドリン含量を測定し、細胞乾燥重量1gあたり1mgの濃度を示しました。
合成されたビンドリンの主な用途は、重要な抗癌剤であるビンクリスチンやビンブラスチンの前駆体としての役割です。カタランタス・ローゼウスの植物中でこれらのアルカロイドは自然界では低い存在量であり、化学合成が困難であるため、合成ビンドリンはこれらの命を救う薬剤の大量生産のための貴重な代替手段となります。
合成ビンドリンの確立された役割を超えて、研究はその潜在的な応用について進行中です:
抗糖尿病特性:研究により、ビンドリンは抗糖尿病特性を持つ可能性があることが示唆されていますが、その治療効果を確認するためにはさらに研究が必要です。
薬剤開発:合成ビンドリンの独特な化学構造は、さまざまな治療用途を持つ新薬の開発に可能性を秘めています。ビンドリン分子を修飾することで、科学者たちはさまざまな病気を対象にした薬剤を創出することができるでしょう。
結論として、ビンドリンの合成は挑戦的で先見的な研究分野を表しています。合成方法の継続的な改良と最適化は、薬剤開発と生産のために重要な技術的支援と指針を提供するでしょう。この分野への興味と探求が促進されることを期待しています。
[1] https://pubchem.ncbi.nlm.nih.gov/compound/260535
[2] https://www.sciencedirect.com/topics/chemistry/vindoline
[3] https://www.nature.com/articles/s42003-021-02617-w
[4] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2531198/
[5] Tsinghua University. A method for producing Vindoline. 2008-12-31.