
분자 구조의 흥미로운 세계에 오신 것을 환영합니다! 오늘은 독특한 특성과 응용 분야를 지닌 SeF6의 Lewis 구조를 탐구하겠습니다. Lewis 구조를 이해하면 SeF6에서 원자들이 어떻게 결합하는지 밝히고 분자의 기하학, 하이브리드화, поля르성을 파악하는 핵심입니다.
리우스 구조는 무엇인가요?
리우스 구조는 Gilbert N. Lewis에 의해 제안된 분자의 전자 배치를 시각적으로 나타내는 방법입니다. 결합 전자를 점으로, 단결합을 선으로 표현하여 리우스 구조는 삼중원칙에 따라 분자의 모양과 특성을 예측합니다. 이 원칙은 원자가 외부 셀프계의 8개의 전자를 가지도록 안정성을 얻기 위해 노력한다는 것을 말합니다. 리우스 구조는 이러한 원칙에 부합하며, 화학 결합에 대한 명확한 그림을 제공합니다.
셀레늄 헥사플루오라이드(SELENIUM HEXAFLUORIDE)는 무엇인가요?
셀레늄 헥사플루오라이드(SeF6)는 투명하고 냄새가 나는 가스로, 하나의 셀레늄 원자와 여섯 개의 플루오린 원자가 결합합니다. 주로 유기 합성에서의 플루오르화제 및 화학 반응의 재료로 사용됩니다. SeF6는 셀레늄 원자에 있는 고유의 유전자 쌍 덕분에 매우 활성화되어 다양한 산업 공정에서 유연하게 사용되는 복합체입니다.
SeF6의 Lewis 구조를 그리는 방법
SeF6의 Lewis 구조 그리는 방법은 다음과 같습니다:
1. 중심 원자를 찾으세요: SeF6에서 셀레늄(Se)은 플루오린보다 덜 전기음성적이므로 중심 원자입니다.
2. 총 전위 전자를 계산하세요: Se는 6개의 전위 전자를, 각 플루오린은 7개의 전위 전자를 공헌하므로, 총 전위 전자는 6 + (6 x 7) = 48 개입니다.
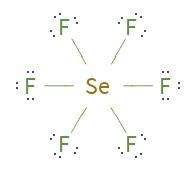
3. 원자 주위에 전자를 배치하세요: 각 플루오린 원자와 중앙 셀레늄 원자 사이에 단일 결합(선)으로 연결하고, 플루오린 원자 주위에 남은 전자를 고립된 쌍으로 배치합니다.
4. 삼중원칙을 만족시키세요: 각 플루오린 원자가 8개의 전자를(2개의 고립된 쌍과 1개의 결합 쌍), 그리고 셀레늄 원자가 12개의 전자를(2개의 고립된 쌍과 6개의 결합 쌍) 가질 때까지 합니다.
5. 공식 заряд을 확인하세요: 모든 원자가 삼중원칙을 충족했기 때문에 공식 заряд 검토가 필요하지 않을 수 있습니다.
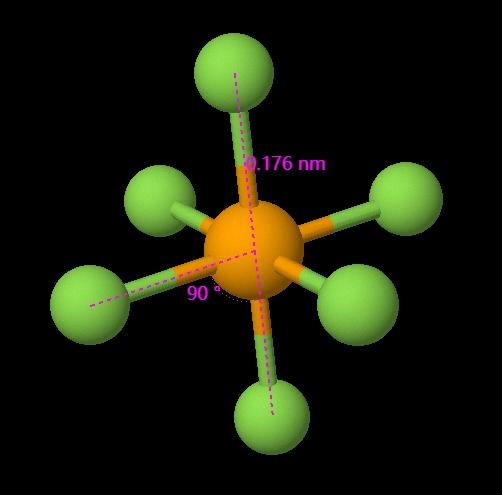
셀레늄 헥사플루오라이드(SeF6)의 분자 기하학
리우스 구조에 따르면 SeF6는 산화물 기하학을 채택합니다. 이 배열에서 6개의 플루오린 원자는 중앙 셀레늄 원자 주위에 대칭적으로 위치하여 6개의 결합 쌍을 형성합니다. 이 기하학은 전자-전자 반발을 최소화하여 안정한 구조를 만듭니다.
셀레늄 헥사플루오라이드(SeF6)의 하이브리드화
SeF6에서 셀레늄 원자는 sp3d2 하이브리드화를 겪습니다. 하나의 s 오비탈, 세 개의 p 오비탈, 두 개의 d 오비탈이 결합하여 6개의 sp3d2 하이브리드 오비탈을 형성합니다. 이 하이브리드 오비탈은 플루오린 원자의 p 오비탈과 교차하여 6개의 강력한 σ 결합을 형성합니다. 이 하이브리드화는 SeF6 분자의 안정성과 대칭성을 보장합니다.
셀레늄 헥사플루오라이드(SeF6)의 극성 여부
셀레늄 헥사플루오라이드(SeF6)는 비극성 분자입니다. 셀레늄(2.55)과 플루오린(3.98) 사이의 전기음성도 차이로 인해 SeF6에는 셀레늄과 플루오린 원자 사이에 극성 공유 결합이 존재하지만, 플루오린 원자들이 중앙의 셀레늄 원자를 대칭적으로 둘러싸고 있어 전체적으로 전기적 쌍극자가 발생하지 않습니다. 결과적으로 SeF6는 비극성 분자 구조를 가지며, 평면적인 대칭성을 띱니다.
셀레늄 헥사플루오라이드(SeF6)의 약한 결합 각도와 결합 길이
SeF6의 결합 각도는 약 90도입니다. 이 각도는 분자의 산화물 기하학에서 유래하는데, 6개의 플루오린 원자가 정규 산화물의 꼭지점에 위치하여 인접한 플루오린 원자 사이에 90도의 결합 각도를 형성합니다. SeF6의 결합 길이는 약 159.7pm입니다.
참고: VSEPR 이론은 분자 기하학과 결합 각도 예측에 좋은 출발점을 제공하지만, 실질적인 분자는 고유의 라운드 패어 반발, 결합极성, 분자의 상호 작용 등의 요인으로 인해 이상적인 각도에서 벗어날 수 있습니다.




