-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here

Pentafluoropyridine, también conocido como perfluoropyridine, tiene el nombre químico de Pentafluoropyridine, CAS: 700-16-3, y la fórmula molecular de C5F5N. Caracteriza un anillo aromático de seis miembros donde cinco átomos de flúor reemplazan todos los átomos de hidrógeno en los átomos de carbono. Como un compuesto perfluoroaromático significativo, la introducción de átomos de flúor y heteroatúmicos en su molécula altera notablemente su estructura y distribución electrónica. Esta modificación imparte propiedades físico-químicas únicas al pentafluoropyridine y afecta su mecanismo de excitación y procesos de relajación. La introducción de átomos de flúor o radicales aumenta la masa del núcleo atómico, lo que reduce la energía de excitación, resultando en un desplazamiento rojo notable en la espectroscopia de absorción en comparación con la benzena. Además, los átomos de flúor mejoran las características de enlace π y antienlace en los anillos aromáticos o heterociclos. Con una mayor cantidad de átomos de flúor, la longitud del enlace C-F disminuye gradualmente, haciendo que la estructura molecular de los compuestos fluorados aromáticos sea más estable y aromática.
La síntesis de pentafluoropyridine fue reportada por primera vez en la década de 1960, involucrando la defluorinación de perfluoropiperidina. En este proceso, se preparó perfluoropiperidina mediante la reacción de la piridina con el hidrógeno difluoruro anhidro en una síntesis electroquímica a altas temperaturas con metales como hierro o níquel. Posteriormente, se obtuvo pentafluoropyridine mediante separación cromatográfica. Cuando se utilizaba el hierro como agente reducible, el rendimiento de pentafluoropyridine era del 26%, mientras que con el níquel, el rendimiento era ligeramente menor al 12%.
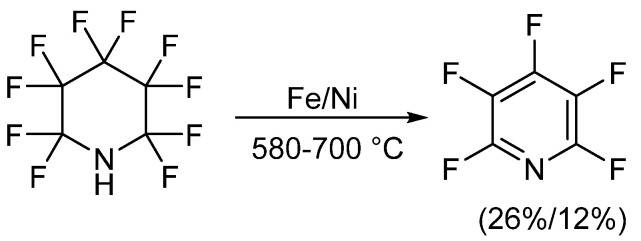
En 1964 y 1965, Chambers et al. y Banks et al. respectivamente publicaron métodos similares para la síntesis de pentafluoropyridine. Los autores calentaron pentachloropyridina y hidrógeno difluoruro anhidro en un recipiente bajo alta presión para producir pentafluoropyridine. Pentachloropyridina se preparó mediante la reacción de la piridina con fosforo pentachloruro. Este método produjo una mezcla de productos, que se pudieron separar mediante destilación.
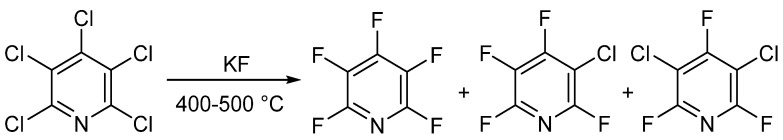
El total de los productos halogénidos fue aproximadamente el 90%, y la proporción del producto podía ajustarse cambiando la temperatura y el tiempo de reacción. Bajo condiciones óptimas, el rendimiento de pentafluoropyridine era del 83%. Este método sigue siendo el estándar de oro para la síntesis comercial de pentafluoropyridine.
Desde mediados de la década de 1960, ha habido poco progreso en los métodos alternativos para la síntesis de pentafluoropiridina. Aproximadamente 20 años después, Banks et al. pirólizaron pentafluoro(triclorometil)benceno y 4-dicloraminotetrafluoropiridina bajo protección de nitrógeno para obtener cantidades traza de pentafluoropiridina. En el mismo año, Coe y Sleigh pirólizaron varias pirrolidinas en presencia de hierro. Esta reacción produjo una mezcla de productos, similar al informe de Banks, con rendimientos muy bajos de pentafluoropiridina (<12%). Más tarde, en 1982, Plevey y colegas lograron un rendimiento del 40% de pentafluoropiridina al fluorurar piridina con tetrafluorocobalto de cesio (III). Sin embargo, también encontraron desafíos, ya que los rendimientos disminuyeron cuando la escala de la reacción superó los 5 gramos.
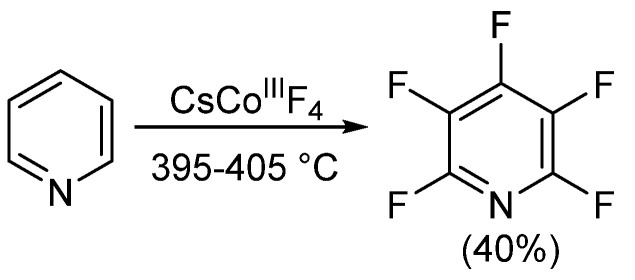
En 2004, Bardin et al. publicaron un ejemplo final donde obtuvieron pentafluoropiridina mediante deshalogenación de C5Cl4F5N en presencia de hierro o zinc. En todos los casos, se obtuvo una mezcla de productos, y el rendimiento no separado fue determinado por análisis GLC, como se muestra en la tabla a continuación.
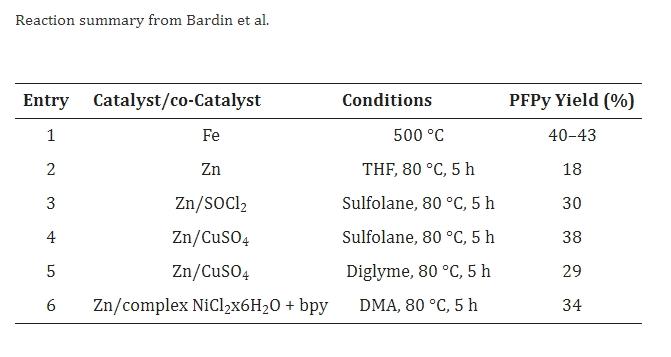
Utilizando 2,4,6-trifluoro-3,5-dicloropiridina como materia prima y KF como agente fluorurante, Zhong Xuhui et al. se centraron en la síntesis de pentafluoropiridina. A través de investigaciones sobre el catalizador de reacción de fluoruración, seleccionaron nuevos catalizadores para reducir la temperatura de reacción, sentando las bases para la industrialización de tales reacciones de fluoruración desafiantes. Al explorar el mecanismo experimental, identificaron un nuevo catalizador de combinación, bromuro de tetrafenilfosfonio y AlCl3 anhidro en una proporción de masa de 3:1, aplicado a la reacción con 2,4,6-trifluoro-3,5-dicloropiridina y KF como agente fluorurante, logrando resultados experimentales favorables. La optimización de los parámetros experimentales dio como resultado: KF: trifluorodicloropiridina: bromuro de tetrafenilfosfonio: AlCl3 = 30g: 150g: 3g: 1g, temperatura de reacción de 240°C, tiempo de reacción de 20 horas, con 3-cloro-tetrafluoropiridina al 15%, pentafluoropiridina al 10%, y selectividad del catalizador al 50%.
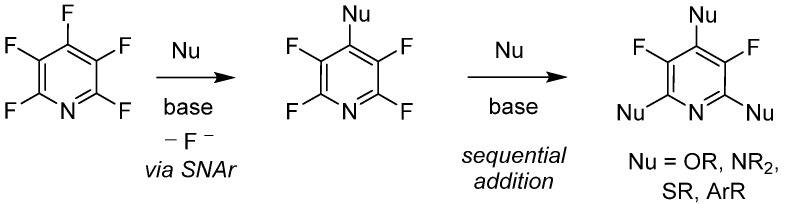
Las transformaciones químicas de la pentafluoropiridina han sido bien documentadas, incluyendo métodos notables como la activación del enlace CF, reacciones de foto-oxidación-reducción, deshidrofluoración y adición nucleofílica. Debido a la variedad de reactivos nucleofílicos, las transformaciones químicas conocidas son altamente flexibles. Además, la pentafluoropiridina exhibe una selectividad regioespecífica única, siendo las adiciones metatéticas en la posición 4 distintivas bajo condiciones básicas suaves, y los reactivos nucleofílicos de tipos O-, N-, S- y C-. También se pueden llevar a cabo adiciones ordenadas 2,6, mientras que la disustitución 3,5 ocurre por separado.
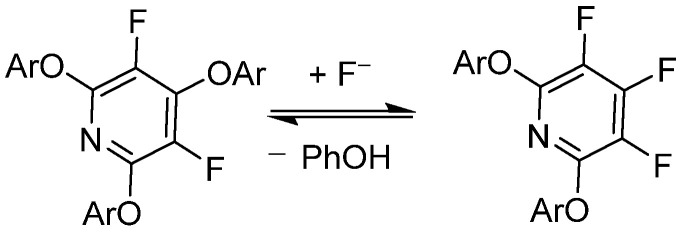
Investigaciones de Vlasov et al. muestran que la pentafluoropiridina puede experimentar reacciones de sustitución reversibles con fluoruros (F?) bajo condiciones básicas, facilitadas por buenos nucleófilos como el fenol. Estudios adicionales utilizando modelado DFT exploraron los efectos de sustitución reversible de éteres aromáticos ricos y pobres en electrones en las posiciones 2,6 de la pentafluoropiridina. Brittain et al. utilizaron estos hallazgos, empleando la pentafluoropiridina como un grupo protector efectivo para varios compuestos fenólicos, que podrían experimentar reacciones de ruptura o desprotección bajo condiciones suaves.
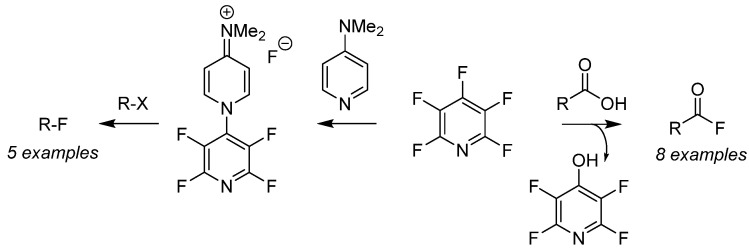
La pentafluoropiridina ha sido utilizada como un reactivo fluorurante nucleofílico para haluros de alquilo (de derecha a izquierda en la figura) y para la desoxigenación de ácidos carboxílicos (de izquierda a derecha en la figura) para preparar piscinas de sustrato multifuncionales. La adición de pentafluoropiridina y N,N-dimetilaminopiridina genera sales de fluoruración estables al aire, permitiendo la fluoruración de haluros orgánicos (R-X). Además, la adición nucleofílica de pentafluoropiridina con ácidos carboxílicos genera fácilmente fluoruros acilo in situ. El intermediario de éster luego se separa del fluoruro no quelado, generando fenol como un subproducto y el fluoruro acilo deseado. Esta estrategia se extiende al uso de pentafluoropiridina como agente de acoplamiento en la síntesis en un solo paso de amidas y ésteres.
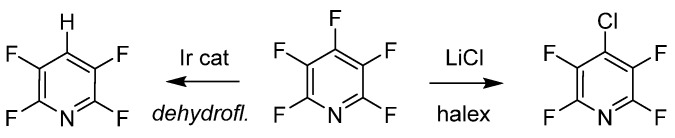
La manipulación intencionada de la pentafluoropiridina incluye deshalogenación selectiva en el sitio y el intercambio de halógenos (halex), como se ilustra. Estos procesos producen sustituciones regioselectivas dependiendo de las condiciones de reacción. Senaweera et al. utilizaron un diseño de reactor de flujo para preparar pentafluoropiridina deshidrofluorinada, logrando una alta rotación fotocatalítica bajo una baja carga de complejo de Ir, demostrando la escalabilidad de tales intermediarios útiles. Se logró el intercambio de sustitución inversa halex en la posición 4 de la pentafluoropiridina con LiCl, con un intercambio adicional con cloro controlado por cinética y termodinámica.
[4] https://baike.baidu.com/item/%E4%BA%94%E6%B0%9F%E5%90%A1%E5%95%B6
 |