-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here


Les structures de Lewis, conçues par Gilbert N. Lewis, représentent visuellement les arrangements des électrons dans les molécules. En représentant les électrons de valence sous forme de points et les liaisons sous forme de lignes, les structures de Lewis prédisent la forme et les propriétés d'une molécule en fonction de la règle de l'octet. Cette règle stipule que les atomes ont tendance à atteindre la stabilité en ayant huit électrons dans leur couche externe. Les structures de Lewis respectent cette règle, offrant ainsi une image claire de la liaison chimique.
L'Chlorate (ClO3^-) est un ion polyatomique avec une masse molaire de 83,49 g/mol. Il se compose d'un atome de chlore lié à trois atomes d'oxygène. L'ion porte une charge négative, ce qui en fait un composant important dans diverses réactions chimiques et applications, telles que la production de désinfectants et d'explosifs. Il est connu pour sa stabilité et ses fortes propriétés oxydantes.
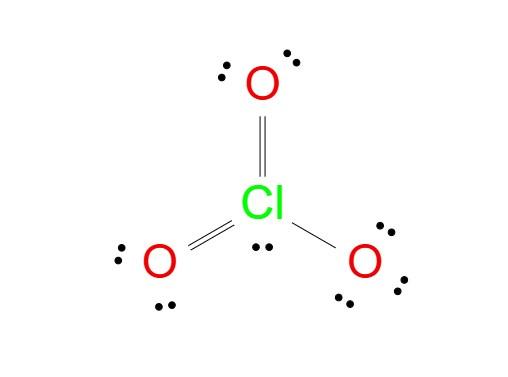
Passons maintenant à la construction de la structure de Lewis de ClO3^- :
Étape 1 : Identifier l'atome central : Le chlore (Cl) est l'atome central dans ClO3^- car il est moins électronégatif que l'oxygène.

Étape 2 : Calculer le total des électrons de valence : Le chlore apporte 7 électrons de valence, et chaque oxygène en apporte 6, ce qui donne un total de 7 + (3 × 6) = 25 électrons de valence. Puisque ClO3^- a une charge de -1, ajoutez un électron de plus, pour un total de 26 électrons de valence.
Étape 3 : Disposer les électrons autour des atomes : Reliez chaque atome d'oxygène à l'atome central de chlore avec une liaison simple (ligne) et répartissez les électrons restants sous forme de paires isolées autour de chaque atome d'oxygène.
Étape 4 : Respecter la règle de l'octet : Assurez-vous que chaque atome d'oxygène possède 8 électrons (2 paires isolées et 1 paire de liaison), et que l'atome de chlore possède 8 électrons (2 paires isolées et 3 paires de liaison).
Étape 5 : Vérifier les charges formelles : Les charges formelles doivent être égales à -1, ce qui indique la structure correcte.
La structure de l'Chlorate comprend un atome de chlore central autour duquel se trouvent 24 électrons, ou 12 paires d'électrons, avec une paire isolée sur l'atome de chlore. Par conséquent, la géométrie moléculaire de ClO3^- sera un plan triangulaire. Il y aura un angle de 109,5 degrés entre les liaisons O-Cl-O.

Cette théorie aborde la répulsion des électrons et le besoin pour les composés d'adopter des formes stables. Dans ClO3^-, trois liaisons sigma se forment entre le chlore et l'oxygène, avec trois paires isolées sur l'atome de chlore. Bien que le chlore n'ait que trois orbitales de valence, la structure de Lewis suggère trois paires de liaisons, ce qui implique l'utilisation des orbitales p dans cette molécule complexe. Des calculs avancés révèlent que la structure électronique consiste en fait en trois liaisons délocalisées à travers tous les quatre atomes, plutôt qu'en trois liaisons distinctes impliquant des orbitales p.
La structure de Lewis suggère que ClO3^- adopte une géométrie de plan triangulaire. Dans cette configuration, les trois atomes d'oxygène sont symétriquement positionnés autour de l'atome central de chlore, formant ainsi trois paires de liaisons. Cette géométrie minimise la répulsion électro-électronique, aboutissant à une configuration stable.
Les orbitales impliquées, ainsi que les liaisons formées lors de l'interaction des molécules de chlore et d'oxygène, seront examinées pour déterminer l'hybridation de l'Chlorate. Les orbitales impliquées sont 3s, 3px, 3py et 3pz. L'atome de chlore, qui est l'atome central dans son état fondamental, aura la configuration 3s23p5 dans sa formation.
Les paires d'électrons dans les orbitales 3s et 3px deviennent non appariées dans l'état excité, et une de chaque paire est promue vers les orbitales 3py et 3pz inoccupées. Les quatre orbitales demi-remplies (une 3s, deux 3p) se hybrident maintenant, produisant quatre orbitales hybrides sp3.
L'angle de liaison dans ClO3^- est d'environ 109,5 degrés. Cet angle résulte de la géométrie de plan triangulaire de la molécule, où les trois atomes d'oxygène sont positionnés aux sommets d'une pyramide trigonal, ce qui donne un angle de liaison de 109,5 degrés entre les atomes d'oxygène adjacents. La longueur de liaison dans ClO3^- est d'environ 170 pm.
| Chlorate (ClO3^-) | |
| Formule moléculaire | ClO3^- |
| Forme moléculaire | Plan triangulaire |
| Polarité | Polar |
| Hybridation | Hybridation sp3 |
| Angle de liaison | 109,5 degrés |
| Longueur de liaison | 170 pm |
Pour déterminer si une structure de Lewis est polaire, examinez la géométrie moléculaire et la polarité des liaisons. Dans le cas de l'Chlorate (ClO3^-), la structure de Lewis montre le chlore au centre lié à trois atomes d'oxygène. ClO3^- a une géométrie de plan triangulaire, où les trois atomes d'oxygène sont disposés de manière asymétrique autour de l'atome de chlore. En conséquence, la molécule est polaire en raison de la distribution inégale de la charge.
Pour calculer l'énergie totale de liaison de ClO3^-, commencez par rechercher l'énergie de liaison pour une seule liaison chlore-oxygène (Cl-O), qui est d'environ 200 kJ/mol. ClO3^- possède trois liaisons Cl-O, donc vous multipliez l'énergie de liaison d'une liaison Cl-O par le nombre de liaisons. Cela donne une énergie totale de liaison de 600 kJ/mol pour ClO3^-. Cette valeur représente l'énergie nécessaire pour rompre toutes les liaisons Cl-O dans une mole de molécules de ClO3^-.
L'ordre de liaison est le nombre de liaisons chimiques entre une paire d'atomes. Dans la structure de Lewis de ClO3^-, chaque liaison chlore-oxygène est une liaison simple, donc l'ordre de liaison pour chaque liaison Cl-O est 1. Si une molécule a des structures de résonance, l'ordre de liaison est moyen entre les différentes structures, mais ClO3^- n'a pas de résonance, donc l'ordre de liaison reste 1.
Les groupes d'électrons dans une structure de Lewis comprennent à la fois les paires de liaison (électrons partagés) et les paires isolées (électrons non liés) autour d'un atome. Dans ClO3^-, chaque atome de chlore possède quatre groupes d'électrons autour de lui, correspondant aux trois liaisons Cl-O (trois paires de liaison et une paire isolée sur le chlore).
Dans une structure de Lewis, les points représentent les électrons de valence. Chaque point correspond à un électron de valence d'un atome. Dans ClO3^-, le chlore est entouré de trois paires de liaison (représentées par des lignes dans la structure de Lewis) et d'une paire isolée (deux points). Chaque atome d'oxygène est représenté par trois paires de points (paires isolées) et une paire de liaison avec le chlore. Les points aident à visualiser comment les électrons sont partagés ou appariés entre les atomes.
Lorsque vous déterminez la meilleure structure de Lewis pour ClO3^-, il est important de prendre en compte à la fois les liaisons et l'agencement des électrons pour garantir la représentation la plus stable. Choisir la structure correcte aide à comprendre ses propriétés et son comportement moléculaire. Si vous explorez comment choisir la meilleure structure de Lewis pour ClO3^- ou d'autres composés, Guidechem fournit un accès à une large gamme de fournisseurs d'Chlorate. Ici, vous pouvez trouver les matières premières idéales pour soutenir vos recherches et applications.
 |