
La structure de Lewis, formulée par Gilbert N. Lewis, représente visuellement la répartition des électrons au sein des molécules. En illustrant les électrons de valence sous forme de points et les liaisons sous forme de traits, ces structures prédirent la forme et les propriétés d'une molécule en se basant sur la règle de l'octet, qui stipule que les atomes cherchent la stabilité en atteignant huit électrons dans leur couche externe.
Le Disulfure de carbone (CS2) est un liquide incolore et inflammable caractérisé par son odeur distinctive. Composé d'un atome de carbone lié à deux atomes de soufre, il présente une structure moléculaire linéaire. Il est principalement utilisé dans la production de colorants, de produits chimiques photographiques et comme solvant.
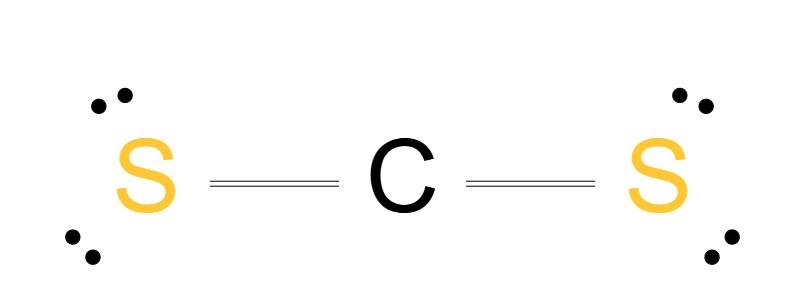
Explorons comment construire la structure de Lewis de CS2 :
Étape 1 : Identifier l'atome central : Le carbone (C) est l'atome central, car il est moins électronégatif que le soufre (S).
Étape 2 : Compter les électrons de valence totaux : Le carbone contribue avec 4 électrons de valence, et chaque atome de soufre contribue avec 6, totalisant 4 + (2 x 6) = 16 électrons de valence.
Étape 3 : Disposer les électrons : Reliez chaque atome de soufre à l'atome de carbone central avec une liaison double (deux traits) et distribuez les électrons restants sous forme de paires isolées autour de chaque atome de soufre.
Étape 4 : Satisfaire la règle de l'octet : Assurez-vous que chaque atome de soufre ait 8 électrons (deux paires isolées et une liaison double), et que l'atome de carbone ait 4 électrons (deux paires isolées et une liaison double).
Étape 5 : Vérifier les charges formelles : Les charges formelles ne sont généralement pas considérées car la règle de l'octet est satisfaite.
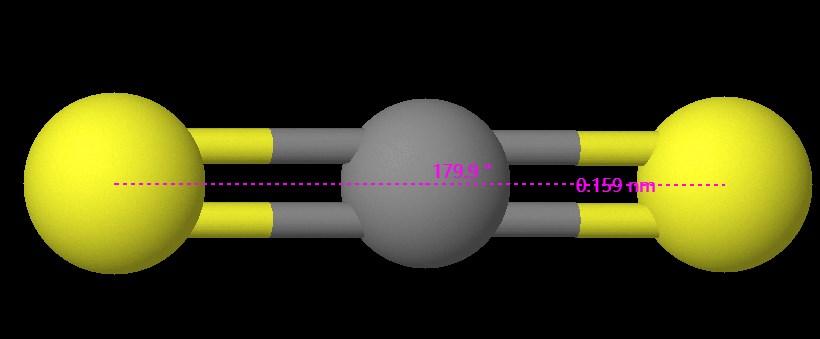
La molécule de CS2 adopte une géométrie linéaire en raison de l'arrangement des paires d'électrons autour de l'atome de carbone central. Avec deux atomes de soufre liés à l'atome de carbone et sans paires isolées, la molécule présente une forme linéaire avec un angle de liaison de 179,9 degrés.
Dans la théorie des orbitales moléculaires, la liaison dans CS2 implique l'overlap des orbitales 2s et 2p des atomes de soufre avec l'orbite 2s de l'atome de carbone. Cela entraîne la formation de deux orbitales moléculaires : l'orbitale de liaison σ2s2p et l'orbitale antiliaison π2p2s. En raison de l'absence de paires isolées, la molécule maintient une géométrie linéaire avec un angle de liaison de 180 degrés.
La géométrie linéaire de CS2 provient de l'arrangement des paires d'électrons autour de l'atome de carbone central, résultant en un angle de liaison de 180 degrés entre les atomes de soufre. Cette configuration minimise la répulsion des électrons et stabilise la molécule.
L'hybridation du carbone dans CS2 implique le mélange des orbitales 2s et 2p pour former deux orbitales hybrides sp. Ces orbitales hybrides se chevauchent ensuite avec les orbitales p des atomes de soufre, facilitant la formation des deux liaisons sigma et la stabilisation de la structure moléculaire linéaire.
Dans CS2, l'angle de liaison est d'environ 179,9 degrés, caractéristique d'une molécule linéaire. La longueur de liaison est d'environ 0,159 nm, ce qui reflète la force des liaisons C-S dans ce composé.
| Disulfure de carbone (CS2) Cas 7783-06-4 | |
| Formule moléculaire | CS2 |
| Forme moléculaire | Linéaire |
| Polarité | Non polaire |
| Hybridation | Hybridation sp |
| Angle de liaison | 179,9 degrés |
| Longueur de liaison | 0,159 nm |
Pour déterminer si une structure de Lewis est polaire, examinez la géométrie moléculaire et la polarité des liaisons. Pour CS2, l'agencement linéaire et la distribution symétrique des paires d'électrons autour de l'atome central de carbone donnent une molécule non polaire, car les moments dipolaires s'annulent.
Pour calculer l'énergie de liaison dans CS2, référez-vous à l'énergie de liaison d'une liaison C-S, qui est d'environ 310 kJ/mol. Étant donné que CS2 contient deux liaisons C-S, vous multipliez l'énergie de liaison par 2, ce qui donne une énergie de liaison totale de 620 kJ/mol pour la molécule CS2.
L'ordre de liaison dans CS2 est déterminé par le nombre de liaisons chimiques entre les atomes. Chaque liaison C-S dans la structure de Lewis représente un ordre de liaison de 1, ce qui reflète la présence d'une seule liaison entre le carbone et le soufre.
Lors de la détermination de la meilleure structure de Lewis pour CS2, il est important de prendre en compte à la fois la liaison et l'agencement des électrons pour garantir la représentation la plus stable. Choisir la bonne structure aide à comprendre ses propriétés et son comportement moléculaire. Si vous explorez comment choisir la meilleure structure de Lewis pour CS2 ou d'autres composés, Guidechem offre un accès à une large gamme de fournisseurs de Disulfure de carbone. Vous y trouverez les matières premières idéales pour soutenir vos recherches et applications.
 |
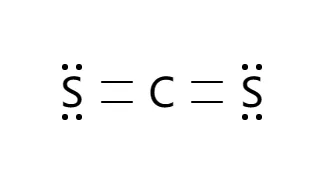 |