-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here


La structure de Lewis, formulée par Gilbert N. Lewis, offre une représentation visuelle des dispositions électroniques au sein des molécules. En illustrant les électrons de valence comme des points et les liaisons comme des lignes, ces structures prédisent la forme et les propriétés d'une molécule, en adhérant à la règle de l'octet, qui stipule que les atomes cherchent la stabilité en atteignant huit électrons dans leur couche externe.
Le trioxyde de sélénium (SeO3) est un composé incolore et volatil composé d'un atome de sélénium lié à trois atomes d'oxygène. Il est largement utilisé dans diverses applications industrielles, notamment pour la production de verre, de papier et comme réactif en synthèse organique.
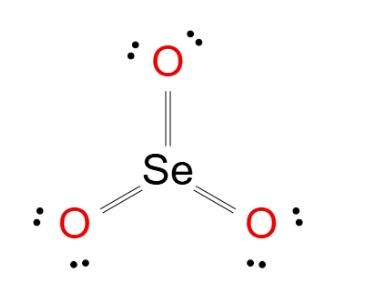
Plongeons dans le processus de création de la structure de Lewis pour le trioxyde de sélénium (SeO3) :
La structure du trioxyde de sélénium comprend un atome central de sélénium entouré par 6 électrons ou 3 paires d'électrons sans paires isolées, donc la géométrie moléculaire de SeO3 est trigonal plane. Les angles de liaison entre les liaisons Se-O sont d'environ 120 degrés.

Cette théorie aborde la répulsion entre électrons et la nécessité pour les composés d'adopter des configurations stables. Dans SeO3, trois liaisons sigma se forment entre le sélénium et l'oxygène, avec trois paires isolées sur chaque atome d'oxygène. Bien que le sélénium n'ait que quatre orbitales de valence, la structure de Lewis suggère trois paires de liaison, impliquant l'utilisation d'orbitales d dans cette complexe. Cependant, les calculs avancés révèlent que la structure électronique comprend en réalité quatre liaisons délocalisées à travers les quatre atomes, plutôt que trois liaisons distinctes impliquant des orbitales d.
La structure de Lewis indique que SeO3 adopte une géométrie trigonale plane. Dans cet arrangement, les trois atomes d'oxygène sont positionnés dans un plan autour de l'atome central de sélénium, formant trois paires de liaison. Cette géométrie minimise la répulsion entre les électrons, conduisant à une configuration stable.
Les orbitales impliquées et les liaisons produites lors de l'interaction entre le sélénium et les atomes d'oxygène seront analysées pour déterminer l'hybridation du trioxyde de sélénium. Les orbitales 3s, 3py, 3pz et 3d sont les orbitales clés impliquées. L'atome de sélénium, qui est l'atome central dans son état fondamental, aura la configuration 3s23p4 lors de sa formation.
Les paires d'électrons dans les orbitales 3s, 3py, 3pz et 3d deviennent désappariées dans l'état excité, avec l'une de chaque paire étant promue vers les orbitales 3d non occupées. Toutes les quatre demi-orbitales (une 3s, une 3py, une 3pz et deux 3d) se mélangent maintenant, produisant la création de quatre orbitales hybrides sp3d.
L'angle de liaison dans SeO3 est d'environ 120 degrés. Cet angle provient de la géométrie trigonale plane de la molécule, où les trois atomes d'oxygène sont positionnés dans un plan autour de l'atome central de sélénium, entraînant des angles de liaison de 120 degrés entre les atomes d'oxygène adjacents. La longueur de liaison dans SeO3 est d'environ 0,155 nm.
| Trioxyde de sélénium (SeO3) | |
| Formule moléculaire | SeO3 |
| Forme moléculaire | Trigonal plane |
| Polarité | Non polaire |
| Hybridation | Hybridation sp3d |
| Angle de liaison | 120 degrés |
| Longueur de liaison | 0,155 nm |
Pour déterminer si une structure de Lewis est polaire, examinez la géométrie moléculaire et la polarité des liaisons. Pour le trioxyde de sélénium (SeO3), la structure de Lewis montre le sélénium au centre lié à trois atomes d'oxygène. SeO3 a une géométrie trigonale plane, avec les trois atomes d'oxygène disposés dans un plan autour de l'atome de sélénium. Bien que les liaisons Se-O soient polaires, la symétrie de la molécule fait que les moments dipolaires s'annulent, rendant SeO3 une molécule non polaire.
Pour calculer l'énergie de liaison totale du trioxyde de sélénium (SeO3), déterminez d'abord l'énergie de liaison pour une seule liaison Se=O, qui est d'environ 498 kJ/mol. Comme SeO3 a trois liaisons Se=O, multipliez l'énergie de liaison d'une liaison Se=O par 3. L'énergie de liaison totale pour SeO3 est donc d'environ 1494 kJ/mol.
 |
 |