-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here

Bienvenue dans le domaine fascinant des structures moléculaires ! Aujourd'hui, plongeons dans la structure de Lewis du Trioxyde de sélénium (SeO3), un composé avec des propriétés intrigantes et une importance en chimie. Comprendre la structure de Lewis du SeO3 fournit des aperçus sur ses liaisons, sa géométrie et d'autres caractéristiques importantes.

Les structures de Lewis, conceptualisées par Gilbert N. Lewis, sont des représentations graphiques de la liaison moléculaire, illustrant l'arrangement des électrons de valence dans les atomes et les molécules. En représentant les paires de liaisons par des lignes et les paires non liées par des points, les structures de Lewis aident à prédire la forme et les propriétés d'une molécule selon la règle de l'octet, qui stipule que les atomes tendent à gagner, perdre ou partager des électrons pour atteindre une configuration électronique stable avec huit électrons dans leur couche extérieure.
Le Trioxyde de sélénium (SeO3) est un composé chimique composé d'un atome de sélénium lié à trois atomes d'oxygène. Il se présente sous forme de solide incolore à température ambiante et est un réactif essentiel dans la synthèse organique, notamment pour l'oxydation des composés organiques.
Explorons comment dessiner la structure de Lewis du SeO3 :
Étape 1 : Déterminer l'atome central : Le sélénium (Se) est l'atome central dans le SeO3 car il peut former plus de liaisons que l'oxygène.
Étape 2 : Calculer le total des électrons de valence : Le sélénium contribue avec 6 électrons de valence, et chaque oxygène contribue avec 6, donnant un total de 6 + (3 x 6) = 24 électrons de valence.
Étape 3 : Disposer les électrons autour des atomes : Connectez chaque atome d'oxygène à l'atome central de sélénium avec une liaison simple (ligne) et distribuez les électrons restants sous forme de paires isolées autour de chaque atome d'oxygène.
Étape 4 : Respecter la règle de l'octet : Assurez-vous que chaque atome d'oxygène a 8 électrons (2 paires isolées et 2 paires de liaisons), et que l'atome de sélénium a 12 électrons (6 paires de liaisons).
Étape 5 : Vérifier les charges formelles : Les charges formelles peuvent ne pas être nécessaires car tous les atomes ont atteint la règle de l'octet.
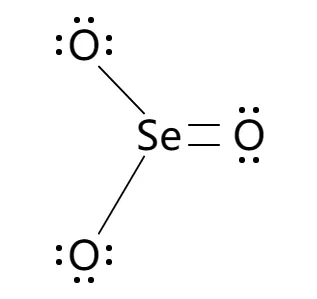
La structure de Lewis suggère que le SeO3 adopte une géométrie pyramidale trigonale. Dans cet agencement, les trois atomes d'oxygène sont positionnés de manière asymétrique autour de l'atome central de sélénium, avec une paire isolée et deux paires de liaisons. Cette géométrie minimise la répulsion entre les électrons, résultant en une configuration stable.

Dans le SeO3, l'atome de sélénium subit une hybridation sp3. Un orbital s et trois orbitaux p se combinent pour former quatre orbitaux hybrides sp3. Ces orbitaux se chevauchent ensuite avec les orbitaux p des atomes d'oxygène, formant quatre liaisons σ fortes. Cette hybridation assure la stabilité et la symétrie de la molécule de SeO3.
Le Trioxyde de sélénium (SeO3) est une molécule polaire. Bien qu'il contienne des liaisons covalentes polaires entre le sélénium et les atomes d'oxygène en raison de la différence d'électroneutralité entre le sélénium (2,55) et l'oxygène (3,44), l'agencement asymétrique des atomes d'oxygène autour de l'atome central de sélénium conduit à un moment dipolaire net, résultant en une polarité moléculaire.
Les angles de liaison dans le SeO3 sont d'environ 107 degrés. Cet angle résulte de la géométrie pyramidale trigonale de la molécule, où la répulsion de la paire isolée force les angles de liaison à être légèrement inférieurs aux 109,5 degrés idéaux. La longueur de liaison entre les atomes de sélénium et d'oxygène est d'environ 160 picomètres.
Remarque : Les angles et longueurs de liaison réels peuvent varier légèrement en raison de facteurs tels que la répulsion des paires isolées et les interactions moléculaires.
| Trioxyde de sélénium Cas 13768-86-0 | |
| Formule moléculaire | SeO3 |
| Forme moléculaire | Pyramidale trigonale |
| Polarité | polaire |
| Hybridation | Hybridation sp3 |
| Angle de liaison | 107 degrés |
| Longueur de liaison | 160 pm |
 |
 |