-
We detected your language preference as English. Would you like to switch to the English version for a better experience?
Switch to English
Stay here


Le tétrafluorure de soufre (SF4) est un composé chimique avec un atome de soufre lié à quatre atomes de fluor. La structure de Lewis du SF4 montre l'arrangement des électrons de valence dans la molécule, suivant la règle de l'octet, qui stipule que les atomes tendent à atteindre la stabilité en ayant huit électrons dans leur couche externe. Cette structure aide à prédire la forme, les propriétés et la liaison de la molécule.
Le tétrafluorure de soufre (SF4) est un gaz incolore et toxique avec une odeur piquante. Il est composé d'un atome de soufre lié covalemment à quatre atomes de fluor. Le SF4 trouve des applications dans la fabrication de semi-conducteurs, comme source de fluor dans diverses réactions et comme réactif dans la synthèse organique.

Dessiner la structure de Lewis du SF4 nécessite de comprendre les électrons de valence et le modèle de liaison entre le soufre et le fluor. Voici les étapes :
La structure de Lewis du SF₄ indique que la molécule a une géométrie moléculaire en forme de bascule. Cette géométrie résulte de la présence d'une paire isolée sur l'atome de soufre et de quatre paires de liaison avec les atomes de fluor, menant à une géométrie en bipyramide trigonale pour les électrons. La paire isolée occupe une position équatoriale, ce qui minimise les répulsions et donne à la molécule sa forme caractéristique en bascule.
Dans le SF4, la théorie des orbitales moléculaires explique la structure électronique de la molécule. Les orbitales moléculaires de liaison et anti-liaison résultent de la combinaison des orbitales atomiques du soufre et du fluor. Les détails exacts des orbitales moléculaires et de leurs énergies dépendent des calculs de mécanique quantique.
Comme mentionné précédemment, la géométrie moléculaire du SF4 est une forme de bascule. Cela résulte de la géométrie bipyramidale trigonal des électrons, avec le soufre au centre et les atomes de fluor aux sommets de la bipyramide, ainsi qu'une paire isolée sur le soufre.
L'hybridation du soufre dans le SF4 peut être déterminée en considérant le nombre de domaines électroniques autour de l'atome de soufre. Avec une paire isolée et quatre paires de liaison, le soufre subit une hybridation sp3d, formant cinq orbitales hybrides qui participent à la liaison.
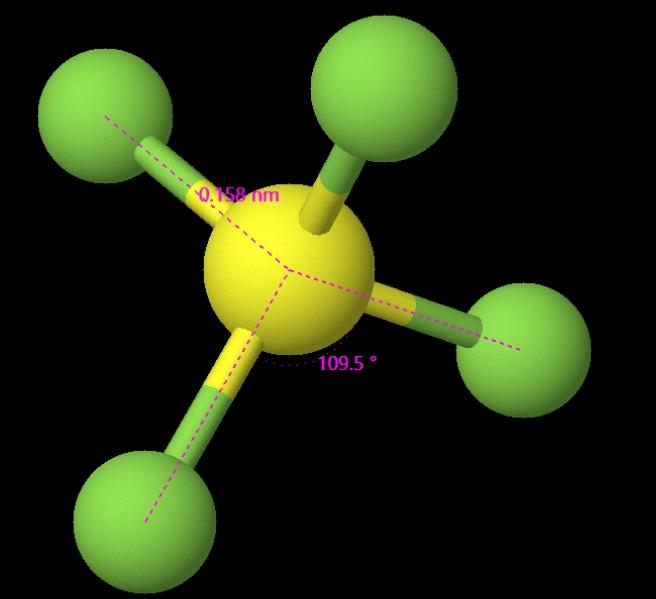
Dans le SF₄, l'angle de liaison F-S-F est d'environ 109,5 degrés. La longueur des liaisons dans le SF₄ est d'environ 0,158 nm pour les liaisons S-F, ce qui reflète les fortes interactions covalentes entre le soufre et le fluor.
| Tétrafluorure de soufre (Numéro CAS : 7783-60-0) | |
| Formule moléculaire | SF4 |
| Forme moléculaire | Bascule |
| Polarité | Polar |
| Hybridation | Hybridation sp3d |
| Angle de liaison | 109,5 degrés |
| Longueur de liaison | 0,158 nm |
Pour déterminer si une structure de Lewis est polaire, examinez la géométrie moléculaire et la polarité des liaisons. Dans le cas du tétrafluorure de soufre (SF₄), la structure de Lewis montre un atome de soufre lié à quatre atomes de fluor. La géométrie moléculaire est en forme de bascule en raison de la présence d'une paire isolée sur l'atome de soufre, ce qui entraîne une distribution asymétrique de la charge. Chaque liaison S-F est polaire car le fluor est plus électronégatif que le soufre, créant des moments dipolaires dans chaque liaison. L'asymétrie globale due à la paire isolée et à l'agencement des atomes de fluor entraîne un moment dipolaire net, rendant le SF₄ une molécule polaire.
L'énergie de liaison peut être estimée en additionnant les énergies de dissociation des liaisons de toutes les liaisons dans la molécule. Pour le SF4, l'énergie de dissociation d'une liaison S-F est d'environ 275 kJ/mol. Comme il y a quatre liaisons S-F, l'énergie totale de liaison est d'environ 1100 kJ/mol.
L'ordre de liaison est calculé comme le nombre de liaisons entre deux atomes divisé par deux. Dans le SF4, chaque liaison soufre-fluor est une liaison simple, donc l'ordre de liaison pour chaque liaison S-F est de 0,5. Cependant, le concept d'ordre de liaison est plus couramment appliqué aux doubles (1) et triples (2) liaisons.
Dans une structure de Lewis, les points représentent les électrons de valence. Chaque point correspond à un électron de valence d'un atome, illustrant comment les électrons sont partagés ou appariés entre les atomes pour former des liaisons.
 |
 |